题目内容
已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂。
(1)请在答卷上用双线桥法标出上述方程式的电子转移方向和数目。
(2) 是还原剂, 是还原产物。
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为 。
(1)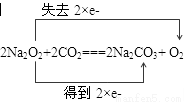 [得失未写或电子数写错均不得分]
[得失未写或电子数写错均不得分]
(2)Na2O2 Na2CO3 (3)33.6L [每空2分]
【解析】
试题分析:(1)过氧化钠与二氧化碳的反应中,过氧化钠既是氧化剂又是还原剂,
(2)过氧化钠既是氧化剂又是还原剂,还原产物是氧化剂发生还原反应后的产物,为Na2CO3
(3)每生成1mol的氧气,则转移2mol电子,当转移3mol电子时会有1.5mol的氧气生成,标准状况下的体积为33.6L
考点:考查氧化还原反应中氧化剂、还原剂、还原产物的判断及双线桥法表示电子转移等

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目