题目内容
5.化学在生活中有着广泛的应用,下列对应关系错误的是( )| 化学性质 | 实际应用 | |
| A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Al2(SO4)3和小苏打在溶液中发生互促水解反应,可生成二氧化碳气体;
B.氯化铁具有强氧化性,可与铜反应;
C.次氯酸盐具有强氧化性,可用于漂白;
D.玻璃含有二氧化硅,HF与SiO2反应.
解答 解:A.Al2(SO4)3水解呈酸性,小苏打水解呈碱性,在溶液中二者发生互促水解反应,可生成二氧化碳气体,可用于泡沫灭火器灭火,故A正确;
B.氯化铁具有强氧化性,可与铜反应,与铁、铜的活泼性无关,故B错误;
C.次氯酸盐具有强氧化性和漂白性,可用于漂白,故C正确;
D.玻璃含有二氧化硅,HF与SiO2反应生成SiF4,氢氟酸可用于雕刻玻璃,故D正确.
故选B.
点评 本题综合考查元素化合物知识,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,难度不大.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
15.实验室模拟“人工树叶”将H2O和CO2转化为O2和C6Hl2O6,以下说法正确的是( )
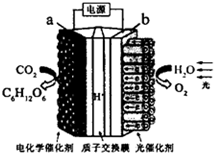

| A. | a极与电源的正极相连 | |
| B. | 该装置能量转化形式仅为电能转化为化学能 | |
| C. | 阳极反应为 6COz+24H+-24e-=C6Hl206+6H20 | |
| D. | 电解后阳极区溶液的pH不变(忽略体积影响) |
16.当干冰气化时,下列所述各项中发生变化的是( )
| A. | 分子间距离 | B. | 范德华力 | C. | 分子内共价键 | D. | 化学性质 |
10.化学与生产和生活密切相关,下列过程中没有发生化学变化的是( )
| A. | 氯气作水的杀菌消毒剂 | B. | 硅胶作袋装食品的干燥剂 | ||
| C. | 二氧化硫作纸浆的漂白剂 | D. | 肥皂水作蚊虫叮咬处的清洗剂 |
2.氧气(O2)和臭氧(O3)是氧元素的两种结构不同的单质.在100kPa时,若要实现下列转化:3O2(g)═2O3(g)将吸收285.0kJ能量.据此,试判断在100kPa压强下,下列结论(或叙述)不正确的是( )
| A. | 氧气比臭氧稳定 | |
| B. | 所有吸热反应不一定都要加热反应才能进行 | |
| C. | 断裂3mol氧气中的化学键吸收的能量大于形成2mol臭氧中的化学键放出的能量 | |
| D. | 3mol氧气的总能量比2mol臭氧的总能量高 |
19.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.
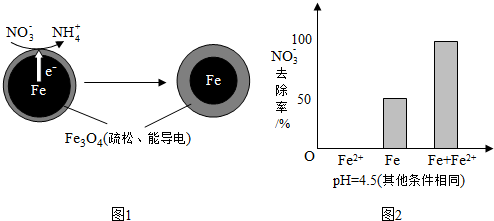
(1)Fe还原水体中NO3-的反应原理如图1所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
pH=4.5时,NO3-的去除率低.其原因是FeO(OH)不导电,阻碍电子转移.
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率.
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如表:
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足.

(1)Fe还原水体中NO3-的反应原理如图1所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 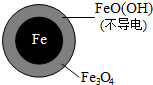 |  |
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率.
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如表:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 约10% | 约3% |
| 1小时pH | 接近中性 | 接近中性 |
8.苯乙烯与溴的四氯化碳溶液反应产物的同分异构体中满足苯环上只有1种氢原子的结构有( )
| A. | 3种 | B. | 4种 | C. | 7种 | D. | 9种 |
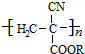 从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下: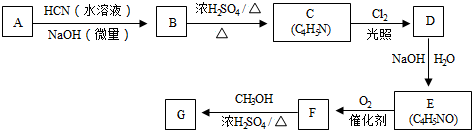
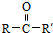 $→_{NaOH(微量)}^{HCN(水溶液)}$
$→_{NaOH(微量)}^{HCN(水溶液)}$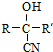
 .其核磁共振氢谱显示为2组峰,峰面积比为1:6.
.其核磁共振氢谱显示为2组峰,峰面积比为1:6. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl.
+NaCl.


