题目内容
| |||||||||||||||||||
解析:
(1) |
答案:2,5,6,2,5,8 精析:根据电子得失总数相等进行配平,配平后的方程式为:2MnO4-+5H2O2+6H+ |
(2) |
答案:淀粉溶液 精析:淀粉溶液和I2混合显蓝色,当加入的Na2S2O3正好和I2反应时,溶液蓝色褪去,可以知道达到滴定终点,所以,该实验可以用淀粉溶液作指示剂. |
(3) |
答案: 精析:用KMnO4滴定待测液,可确定其中H2O2的物质的量为2.5×10-3a1b1. 向待测液中加入过量KI并做适当处理后,用Na2S2O3滴定,可知生成I2的物质的量为0.5×10-3a2b2,其中H2O2氧化生成的I2的物质的量为2.5×10-3a1b1,则CH3COOOH氧化生成的I2的物质的量为0.5×10-3a2b2-2.5×10-3a1b1,所以原b0 mL待测液中CH3COOOH的浓度为 |
(4) |
答案:否 精析:过量的KI不影响Na2S2O3和I2的反应,所以对结果没有影响. |

 名校课堂系列答案
名校课堂系列答案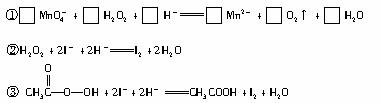
 MnO4- +
MnO4- +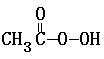 + 2I- + 2 H+ ═ CH3COOH + I2 + 2 H2O
+ 2I- + 2 H+ ═ CH3COOH + I2 + 2 H2O MnO4-
+
MnO4-
+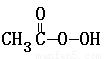 + 2I-
+ 2 H+ ═ CH3COOH + I2
+ 2 H2O
+ 2I-
+ 2 H+ ═ CH3COOH + I2
+ 2 H2O