题目内容
同温同压下的O2和H2,若体积相同,则两种气体的物质的量之比为
1:1
1:1
,分子个数之比为1:1
1:1
.分析:同温同压下,气体摩尔体积相同,根据n=
计算两种气体的物质的量之比,根据N=
NA计算其分子个数之比.
| V |
| Vm |
| V |
| Vm |
解答:解:同温同压下,气体摩尔体积相同,根据n=
知,当体积相等时,其物质的量之比为1:1,根据N=
NA知,当体积相等时,其分子个数之比为1:1,
故答案为:1:1;1:1.
| V |
| Vm |
| V |
| Vm |
故答案为:1:1;1:1.
点评:本题考查了阿伏伽德罗定律及其推论,根据n=
、N=
NA来分析解答即可,注意有关气体体积的计算首先必须温度和压强相同,否则无法比较.
| V |
| Vm |
| V |
| Vm |

练习册系列答案
相关题目
下列关于反应过程中能量变化的说法正确的是( )


| A、在一定条件下,某可逆反应的△H=+100kJ?mol-1,则该反应正反应活化能比逆反应活化能大100kJ?mol-1 | B、图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0未使用和使用催化剂时,反应过程中的能量变化 | C、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | D、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2 |
 运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.
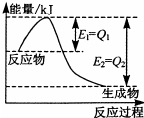
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义. cC(气)+dD(气);ΔH=Q,根据图回答:
cC(气)+dD(气);ΔH=Q,根据图回答: