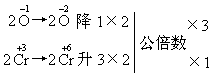题目内容
针对以下A~D四个涉及H2O2的反应(未配平)填写空白
A.Na2O2+HCl![]() H2O2+NaCl
H2O2+NaCl
B.Ag2O+H2O2![]() Ag+O2+H2O
Ag+O2+H2O
C.H2O2![]() +H2O+O2
+H2O+O2
D.H2O2+Cr2(SO4)3+KOH![]() K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填代号)________,该反应配平的化学方程式为________.
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)________.
(3)H2O2体现弱酸性的反应是(填代号),其理由为________.
答案:
解析:
解析:
|
解析: 本题考查两个问题,一是从元素的化合价是否有变化判断反应的类型,由此分析物质的性质.二是氧化还原反应方程式的配平.A反应中元素的化合价无变化,是个离子反应,由强酸HCl溶液制得弱酸H2O2.B、C、D三个反应中H2O2中氧元素的化合价都发生了变化,B中 H2O2+Cr2(SO4)3+KOH 3H2O2+Cr2(SO4)3+10KOH |

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目