题目内容
 (2011?安徽)科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
(2011?安徽)科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )分析:根据信息中该分子中N-N-N键角都是108.1°及N(NO2)3的结构应与氨气相同,则分子中四个氮原子不共平面,利用元素的化合价来分析其性质,利用是否同种元素之间形成共用电子对来分析极性键.
解答:解:A、N(NO2)3是一种共价化合物,N、O原子之间形成的化学键是极性键,故A正确;
B、根据题干信息知该分子中N-N-N键角都是108.1°,推知分子中4个氮原子在空间呈四面体型,
所以分子中四个氧原子不可能共平面,故B错误;
C、该分子中的氮既有+3价也有+5价,+3价氮既有氧化性又有还原性,故C正确;
D、N(NO2)3的相对分子质量为152,15.2 g N(NO2)3为0.1mol,该物质的分子中所含原子为1NA即6.02×1023个原子,故D错误.
故选:C.
B、根据题干信息知该分子中N-N-N键角都是108.1°,推知分子中4个氮原子在空间呈四面体型,
所以分子中四个氧原子不可能共平面,故B错误;
C、该分子中的氮既有+3价也有+5价,+3价氮既有氧化性又有还原性,故C正确;
D、N(NO2)3的相对分子质量为152,15.2 g N(NO2)3为0.1mol,该物质的分子中所含原子为1NA即6.02×1023个原子,故D错误.
故选:C.
点评:作为2011年的安徽理综高考题,题干信息比较新颖,同时考查大家熟悉的化学键、分子结构、氧化还原反应和物质的量的相关计算.

练习册系列答案
相关题目
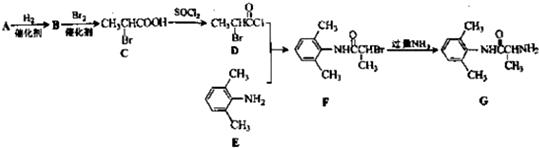
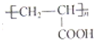 的单体,则A中含有的官能团是
的单体,则A中含有的官能团是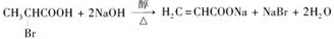
 、
、