题目内容
(2011?南京三模)短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是( )
分析:短周期元素A、B、C的原子序数依次递增,B原子的最外层电子数等于A原子的次外层电子数,最外层电子数不超过8,故A有2个电子层,B的最外层电子数为2,A与C同主族,它们的原子最外层电子数之和为10,则A、C的最外层电子数为
=4,则A为碳元素、C为Si元素,B元素的原子序数大于碳元素,最外层电子数为2,则B为Mg元素,据此解答.
| 10-2 |
| 2 |
解答:解:短周期元素A、B、C的原子序数依次递增,B原子的最外层电子数等于A原子的次外层电子数,最外层电子数不超过8,故A有2个电子层,B的最外层电子数为2,A与C同主族,它们的原子最外层电子数之和为10,则A、C的最外层电子数为
=4,则A为碳元素、C为Si元素,B元素的原子序数大于碳元素,最外层电子数为2,则B为Mg元素,
A.同主族自上而下原子半径增大,同周期自左而右原子半径减小,故原子半径Mg>Si>C,故A错误;
B.同主族自上而下非金属性减弱,故非金属性C>Si,非金属性越强氢化物越稳定,故氢化物稳定性A>C,故B正确;
C.氧化镁与水不反应,不能化合生成氢氧化镁,可由可溶性镁盐与碱反应制得.二氧化硅与水不反应,不能化合生成硅酸,由可溶性硅酸盐与酸反应制备硅酸,故C错误;
D.工业上可以利用碳为还原剂,利用热还原法冶炼镁,工业制备硅:C+SiO2
Si+2CO↑,故D正确;
故选BD.
| 10-2 |
| 2 |
A.同主族自上而下原子半径增大,同周期自左而右原子半径减小,故原子半径Mg>Si>C,故A错误;
B.同主族自上而下非金属性减弱,故非金属性C>Si,非金属性越强氢化物越稳定,故氢化物稳定性A>C,故B正确;
C.氧化镁与水不反应,不能化合生成氢氧化镁,可由可溶性镁盐与碱反应制得.二氧化硅与水不反应,不能化合生成硅酸,由可溶性硅酸盐与酸反应制备硅酸,故C错误;
D.工业上可以利用碳为还原剂,利用热还原法冶炼镁,工业制备硅:C+SiO2
| ||
故选BD.
点评:本题考查结构性质位置关系、元素周期律、元素化合物性质等,难度中等,推断元素是解题关键,B原子的最外层电子数等于A原子的次外层电子数是推断突破口.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目

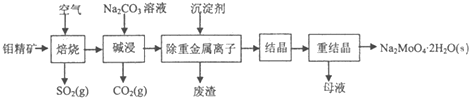
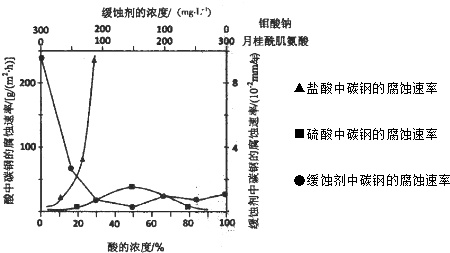
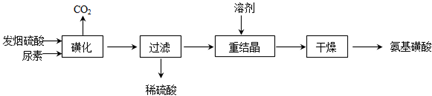
 (2011?南京三模)核能源已日益成为当今世界的主要能源.
(2011?南京三模)核能源已日益成为当今世界的主要能源.