��Ŀ����
ͬѧΪ̽��̼���ε����ʣ���װ��10mL 0.01mol?L-1 Na2CO3��Һ��X�Թܺ�װ��10mL 0.01mol?L-1NaHCO3��Һ��Y�Թ��У��ֱ���εμ�15mL 0.01mol?L-1�����ᣮ
��1����Ӧ��X�Թ��е������� ��
��2����Ӧ�� ����X��Y���Թ��в�����������٣����������Թ��зֱ����10mL 0.01mol?L-1�����ᣬ���Թ������ղ��������� ���X�ࡱ����Y�ࡱ��һ���ࡱ����
��1����Ӧ��X�Թ��е�������
��2����Ӧ��
���㣺̽��̼������̼�����Ƶ�����
ר�⣺Ԫ�ؼ��仯����
��������1��n��Na2CO3��=0.01L��0.01mol/L=0.0001mol��n��HCl��=0.00015mol��X���ȷ���Na2CO3+HCl=NaHCO3+NaCl������NaHCO3+HCl=NaCl+H2O+CO2����
��2��n��NaHCO3��=0.01L��0.01mol/L=0.0001mol�����Na2CO3+2HCl=H2O+CO2��+2NaCl��NaHCO3+HCl=NaCl+H2O+CO2�����㣮
��2��n��NaHCO3��=0.01L��0.01mol/L=0.0001mol�����Na2CO3+2HCl=H2O+CO2��+2NaCl��NaHCO3+HCl=NaCl+H2O+CO2�����㣮
���
�⣺��1��n��Na2CO3��=0.01L��0.01mol/L=0.0001mol��n��HCl��=0.0015mol����
Na2CO3+HCl=NaHCO3+NaCl
0.0001 0.0001 0.0001 0.0001
NaHCO3+HCl=NaCl+H2O+CO2��
0.00005 0.00005
��Ӧ������ΪNaCl��NaHCO3��
�ʴ�Ϊ��NaCl��NaHCO3��
��2��������������֪��X��X�ȷ���Na2CO3+HCl=NaHCO3+NaCl������NaHCO3+HCl=NaCl+H2O+CO2������������Ϊ0.00005mol��
Y��n��NaHCO3��=0.01L��0.01mol/L=0.0001mol������NaHCO3+HCl=NaCl+H2O+CO2�������������������Ϊ0.0001mol����X�����������٣�
���������Թ��зֱ����10mL 0.01mol?L-1�����ᣬ�������������Na2CO3+2HCl=H2O+CO2��+2NaCl��NaHCO3+HCl=NaCl+H2O+CO2����n��Na2CO3��=n��NaHCO3��=n��CO2�����������ɵ�����һ���࣬
�ʴ�Ϊ��X��һ���࣮
Na2CO3+HCl=NaHCO3+NaCl
0.0001 0.0001 0.0001 0.0001
NaHCO3+HCl=NaCl+H2O+CO2��
0.00005 0.00005
��Ӧ������ΪNaCl��NaHCO3��
�ʴ�Ϊ��NaCl��NaHCO3��
��2��������������֪��X��X�ȷ���Na2CO3+HCl=NaHCO3+NaCl������NaHCO3+HCl=NaCl+H2O+CO2������������Ϊ0.00005mol��
Y��n��NaHCO3��=0.01L��0.01mol/L=0.0001mol������NaHCO3+HCl=NaCl+H2O+CO2�������������������Ϊ0.0001mol����X�����������٣�
���������Թ��зֱ����10mL 0.01mol?L-1�����ᣬ�������������Na2CO3+2HCl=H2O+CO2��+2NaCl��NaHCO3+HCl=NaCl+H2O+CO2����n��Na2CO3��=n��NaHCO3��=n��CO2�����������ɵ�����һ���࣬
�ʴ�Ϊ��X��һ���࣮
���������⿼��̼���ơ�̼�����Ƶ�����ʵ�飬Ϊ��Ƶ���㣬���շ����ķ�Ӧ���Ⱥ�˳��Ϊ���Ĺؼ������ط�������������Ŀ��飬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
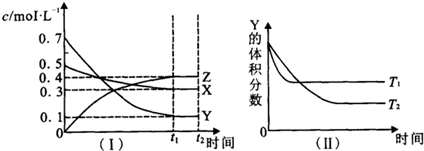
T��ʱ��������X������Y����һ�ܱ������У���Ӧ��������Z����Ӧ�����и����ʵ� Ũ�ȱ仯��ͼ������ʾ�����������������䣬��T1��T2�����¶��£�Y����������仯��ͼ������ʾ�����н�����ȷ���ǣ�������

| A��ͼ������T1��T2��������Ӧ�����ȷ�Ӧ |
| B��t2 minʱ������ѹǿ���䣬ͨ��ϡ�����壬ƽ��������Ӧ�����ƶ� |
| C�������������䣬�����¶ȣ������淴Ӧ���ʾ�������X��ת�������� |
| D��T��ʱ�����ܱ������и�������ʼŨ��Ϊ��0.4mol?L-1 X��0.4mol?L-1 Y��0.2mol/L Z���������������䣬�ﵽƽ��ʱz��Ũ��Ϊ0.4 mol?L-1 |
���෨��ѧϰ���о���ѧ��һ�ֳ��õĿ�ѧ���������з���������ǣ�������
| A�����ݷ����к��е���ԭ�ӵĸ��������ΪһԪ�ᡢ��Ԫ��� |
| B�����ݷ�Ӧ�е������仯������ѧ��Ӧ��Ϊ�������ϣ��ֽ⣬�û������ֽ⡱���� |
| C��������Һ����������ǿ����������ʷ�Ϊǿ����ʺ�������� |
| D��KOH��NH3?H2O���Ǽ� |
�������ӷ���ʽ��ȷ���ǣ�������
| A��Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O |
| B����NaHCO3��Һ�м�������Ca��OH��2��Һ��2HCO+Ca2++2OH-�TCaCO3��+CO32-+2H2O |
C������Һ�еμ�Na2CO3��Һ�� |
| D�����Ȼ�������Һ�еμ�ϡ���Fe2++2H++NO�TFe3++NO2��+H2O |
