题目内容
4.12.5g CuSO4•5H2O中含有0.05mol CuSO4,有0.25mol H2O,有0.05NA个Cu,有0.45NA个O,有6.35NA个电子,有6.35mol质子.分析 依据n=$\frac{m}{M}$计算五水硫酸铜的物质的量,结合1mol五水硫酸铜含有5mol水,1mol铜离子,9mol氧原子,127mol电子,127mol质子,据此解答.
解答 解:12.5g CuSO4•5H2O物质的量为:$\frac{12.5g}{250g/mol}$=0.05mol,含有水分子的物质的量为0.05mol×5=0.25mol;含有铜物质个数为:0.05mol×NA=0.05NA;含有氧原子个数为:0.05mol×9×NA=0.45NA;含有质子数=电子数=127×0.05mol=6.35mol;个数为6.35NA;
故答案为:0.05;0.25;0.05NA;0.45NA;6.35NA;6.35.
点评 本题考查了有关物质的量计算,侧重考查物质所含微粒数目的计算,明确以物质的量为核心的计算公式及物质的组成与结构是解题关键,题目难度不大.

练习册系列答案
相关题目
12.100mL0.6mol•L-1盐酸加到等体积0.4mol•L-1NaOH溶液中,所得溶液中的 pH值是( )
| A. | 0.2 | B. | 0.7 | C. | 1.0 | D. | 2.0 |
9.下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100 ml 0.5 mol/L MgCl2 溶液 | B. | 200 ml 0.25 mol/L CaCl2溶液 | ||
| C. | 50 ml 1 mol/L NaCl溶液 | D. | 200 ml 0.25 mol/L HCl溶液 |
16.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 酸雨的形成CO2+H2O═H2CO3化合反应 | |
| B. | 干粉灭火器的反应原理6NaHCO3+2Al2(SO4)3═3Na2SO4+6CO2↑+Al(OH)3↓复分解反应 | |
| C. | 用稀硫酸洗去附着在试管壁上的铜Cu+H2SO4═CuSO4+H2↑ 置换反应 | |
| D. | 误服用氯化钡后用硫酸镁解毒BaCl2+MgSO4═MgCl2+BaSO4↓ 复分解反应 |
13.下列各选项中所述的两个量,前者一定大于后者的是( )
| A. | 0.10mol•L-1的醋酸溶液和0.01mo•L-1的醋酸溶液中水的电离度 | |
| B. | 将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量 | |
| C. | 物质的量浓度相等的(NH4)2SO4溶液和(NH4)2SO3溶液中NH4+的浓度 | |
| D. | 物质的量浓度相等的CH3COONa溶液和 Na2CO3溶液的pH |
14.下列实验操作中错误的是( )
| A. | 用四氯化碳萃取碘水中的碘的实验,分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 蒸发结晶时剩余少量液体停止加热 | |
| D. | 称量时,称量物放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
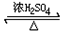 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.