题目内容
某温度、压强下,将一定量反应物通入密闭容器进行反应
SiCl4(g)+2H2(g)Si(s)+4HCl(g);ΔH=+QkJ·mol-1(Q>0),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.若单位时间内生成x molHCl的同时,生成x molH2,则反应达到平衡状态
D.使用过量的H2或升高温度都可以提高SiCl4的转化率
D
解析:根据反应式可判断,该反应是体积增大的、吸热的可逆反应。增大压强平衡向逆反应方向移动,反应物的转化率降低,A不正确。因为是可逆反应,转化率不可能是100%的,所以吸热的热量要小于QkJ,B不正确。C中的反应速率方向是相反的,但不满足速率之比是相应的化学计量数之比,所以也是错误的,增大氢气的浓度,平衡向正反应方向移动,升高温度平衡也向正反应方向移动,所以都可以提该四氯化硅的转化率,正确的答案是D。

练习册系列答案
相关题目
 I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中, 2X
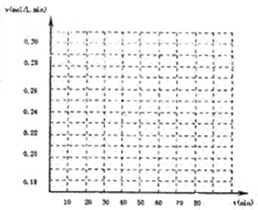
2X 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是


 Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0  Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0) Si3N4(s) +
12HCl(g) △H<0
Si3N4(s) +
12HCl(g) △H<0  Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)