题目内容
15.下列装置或操作正确且能达到实验目的是( )| A. |  加热分解NaHCO3 | B. |  除去氯气中的少量氯化氢 | ||
| C. |  构成铜锌原电池 | D. |  分馏石油 |
分析 A.碳酸氢钠不稳定,加热时注意试管口略朝下;
B.二者都与硝酸银溶液反应;
C.锌置换出铜;
D.温度计位置错误.
解答 解:A.碳酸氢钠不稳定,加热易分解,装置正确,可完成实验,故A正确;
B.氯气与水反应生成盐酸,二者都与硝酸银溶液反应,应用饱和食盐水,故B错误;
C.锌置换出铜,应将锌放在盛有硫酸锌的烧杯中,故C错误;
D.温度计用于测量馏分的温度,应位于蒸馏烧瓶的支管口,故D错误.
故选A.
点评 本题考查较为综合,涉及物质的分离、制备以及原电池等知识,为高考常见题型,侧重学生的分析、实验能力的考查,注意把握实验的严密性以及合理性的评价,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列叙述正确的是( )
| A. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH | |
| B. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| C. | 在铁件上镀铜时,金属铜作阴极 | |
| D. | 电解精炼铜时,电解质溶液中铜离子浓度保持不变 |
6.下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是( )
| A. | Cu2+ K+ Na+ SO42- | B. | K+ Na+ Cl-HCO3- | ||
| C. | Cl- NO3- Mg2+ NH4+ | D. | NO3- Na+ Cl-K+ |
3.能在水溶液中大量共存的一组离子是( )
| A. | K+、H+、NO3-、SiO32- | B. | H+、NH4+、Al3+、SO42- | ||
| C. | Fe2+、H+、ClO-、SO42- | D. | AlO2-、Mg2+、HCO3-、NO3- |
20.下列高分子化合物所对应的结构单元正确的是( )
| A. | 聚氯乙烯  | B. | 聚苯乙烯  | ||
| C. | 聚异戊二烯 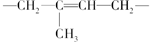 | D. | 聚丙烯-CH2-CH2-CH2- |
4.从下列实验事实所引出的相应结论正确的是( )
| 选项 | 实 验 事 实 | 结 论 |
| A | BaSO4难溶于水,NH3的水溶液导电 | BaSO4是非电解质,NH3是电解质 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | 等体积,H+浓度相同的盐酸和醋酸同时分别与少量等质量的形状相同的锌粒反应 | 产生氢气的质量相同 |
| D | 在容积可变的密闭容器中发生反应: H2(g)+I2(g)?2HI(g),把容积缩小一倍 | 正反应速率加快,逆反应速率不变 |
| A. | A | B. | B | C. | C | D. | D |
 .该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.
.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.