��Ŀ����
0.2mol�л����0.4mol O2���ܱ�������ȼ�պ�IJ���ΪCO2��CO��H2O��g�������ᆳ��Ũ�����Ũ�������������10.8g����ͨ������CuO��ַ�Ӧ������������3.2g�����������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6g����1��ȼ�պ�IJ�������ʵ����ֱ�ΪCO2 mol��CO mol��H2O��g�� mol��
��2���ƶϸ��л���Ļ�ѧʽΪ ��
��3������˴Ź���������ʾֻ�����ֻ�����ͬ��H����ȷ�����л���Ľṹ��ʽΪ ��
���𰸡���������1��Ũ�������������10.8gΪ�л���ȼ������ˮ������������n=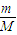 ����ˮ�����ʵ�����
����ˮ�����ʵ�����
����ͨ������CuO��������ӦCuO+CO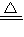 Cu+CO2�����ݲ����������л���ȼ�����ɵ�CO�����ʵ�����
Cu+CO2�����ݲ����������л���ȼ�����ɵ�CO�����ʵ�����
���ݷ�ӦCuO+CO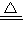 Cu+CO2����CO��CuO��Ӧ���ɵĶ�����̼���������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼�������������л���ȼ�����ɵĶ�����̼��CO��CuO��Ӧ���ɵĶ�����̼���ݴ˼��㣻
Cu+CO2����CO��CuO��Ӧ���ɵĶ�����̼���������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼�������������л���ȼ�����ɵĶ�����̼��CO��CuO��Ӧ���ɵĶ�����̼���ݴ˼��㣻
��2�����ݣ�1�����л���ȼ�����ɵ�CO2��CO��H2O��g�����ʵ���������Ԫ���غ㣬����0.2mol�л��ﺬ�е�Ԫ��ԭ�ӵ����ʵ������ݴ���д��ѧʽ��
��3���˴Ź���������ʾֻ�����ֻ�����ͬ��H������л���ķ���ʽ�ж��л���Ľṹʽ��
����⣺��1��Ũ�������������10.8gΪ�л���ȼ������ˮ������������ˮ�����ʵ���Ϊ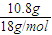 =0.6mol��
=0.6mol��
������CuO��ַ�Ӧ������������3.2g�����л���ȼ�����ɵ�CO�����ʵ���Ϊx����
CuO+CO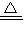 Cu+CO2�������������١�m
Cu+CO2�������������١�m
1mol 16g
x 3.2g
����x=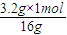 =0.2mol��
=0.2mol��
�������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼��������������̼���ʵ���Ϊ =0.4mol��
=0.4mol��
���ɷ�ӦCuO+CO Cu+CO2��֪��0.2molCO��CuO��Ӧ���ɵĶ�����̼�����ʵ���Ϊ0.2mol�������л���ȼ�����ɵĶ�����̼Ϊ0.4mol-0.2mol=0.2mol��
Cu+CO2��֪��0.2molCO��CuO��Ӧ���ɵĶ�����̼�����ʵ���Ϊ0.2mol�������л���ȼ�����ɵĶ�����̼Ϊ0.4mol-0.2mol=0.2mol��
�ʴ�Ϊ��0.2��0.2��0.6��
��2��0.2mol����0.4molO2����0.2molCO2��0.2molCO��0.6molH2O��g����
����0.2mol�л��ﺬ��Cԭ��Ϊ0.2mol+0.2mol=0.4mol������Hԭ��Ϊ0.6mol×2=1.2mol������Oԭ��Ϊ0.2mol×2+0.2mol+0.6mol-0.4mol×2=0.4mol����1mol�л��ﺬ��Cԭ��Ϊ2mol������Hԭ��Ϊ6mol������Oԭ��Ϊ2mol�������л���Ļ�ѧʽΪC2H6O2���ʴ�Ϊ��C2H6O2��
��3���л���ķ���ʽΪC2H6O2���˴Ź���������ʾֻ�����ֻ�����ͬ��H�����л���Ϊ�Ҷ������ṹ��ʽΪHOCH2CH2OH���ʴ�Ϊ��HOCH2CH2OH��
���������⿼���л������ʽ��ȷ�����ѶȲ���ע�����Ԫ���غ����ж��л���ķ���ʽ�е����ã�
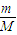 ����ˮ�����ʵ�����
����ˮ�����ʵ���������ͨ������CuO��������ӦCuO+CO
 Cu+CO2�����ݲ����������л���ȼ�����ɵ�CO�����ʵ�����
Cu+CO2�����ݲ����������л���ȼ�����ɵ�CO�����ʵ��������ݷ�ӦCuO+CO
 Cu+CO2����CO��CuO��Ӧ���ɵĶ�����̼���������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼�������������л���ȼ�����ɵĶ�����̼��CO��CuO��Ӧ���ɵĶ�����̼���ݴ˼��㣻
Cu+CO2����CO��CuO��Ӧ���ɵĶ�����̼���������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼�������������л���ȼ�����ɵĶ�����̼��CO��CuO��Ӧ���ɵĶ�����̼���ݴ˼��㣻��2�����ݣ�1�����л���ȼ�����ɵ�CO2��CO��H2O��g�����ʵ���������Ԫ���غ㣬����0.2mol�л��ﺬ�е�Ԫ��ԭ�ӵ����ʵ������ݴ���д��ѧʽ��
��3���˴Ź���������ʾֻ�����ֻ�����ͬ��H������л���ķ���ʽ�ж��л���Ľṹʽ��
����⣺��1��Ũ�������������10.8gΪ�л���ȼ������ˮ������������ˮ�����ʵ���Ϊ
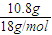 =0.6mol��
=0.6mol��������CuO��ַ�Ӧ������������3.2g�����л���ȼ�����ɵ�CO�����ʵ���Ϊx����
CuO+CO
 Cu+CO2�������������١�m
Cu+CO2�������������١�m1mol 16g
x 3.2g
����x=
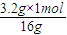 =0.2mol��
=0.2mol���������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6gΪ������̼��������������̼���ʵ���Ϊ
 =0.4mol��
=0.4mol�����ɷ�ӦCuO+CO
 Cu+CO2��֪��0.2molCO��CuO��Ӧ���ɵĶ�����̼�����ʵ���Ϊ0.2mol�������л���ȼ�����ɵĶ�����̼Ϊ0.4mol-0.2mol=0.2mol��
Cu+CO2��֪��0.2molCO��CuO��Ӧ���ɵĶ�����̼�����ʵ���Ϊ0.2mol�������л���ȼ�����ɵĶ�����̼Ϊ0.4mol-0.2mol=0.2mol���ʴ�Ϊ��0.2��0.2��0.6��
��2��0.2mol����0.4molO2����0.2molCO2��0.2molCO��0.6molH2O��g����
����0.2mol�л��ﺬ��Cԭ��Ϊ0.2mol+0.2mol=0.4mol������Hԭ��Ϊ0.6mol×2=1.2mol������Oԭ��Ϊ0.2mol×2+0.2mol+0.6mol-0.4mol×2=0.4mol����1mol�л��ﺬ��Cԭ��Ϊ2mol������Hԭ��Ϊ6mol������Oԭ��Ϊ2mol�������л���Ļ�ѧʽΪC2H6O2���ʴ�Ϊ��C2H6O2��
��3���л���ķ���ʽΪC2H6O2���˴Ź���������ʾֻ�����ֻ�����ͬ��H�����л���Ϊ�Ҷ������ṹ��ʽΪHOCH2CH2OH���ʴ�Ϊ��HOCH2CH2OH��
���������⿼���л������ʽ��ȷ�����ѶȲ���ע�����Ԫ���غ����ж��л���ķ���ʽ�е����ã�

��ϰ��ϵ�д�
�����Ŀ