ћвƒњƒЏ»Ё
“‘ЄїЇђЅтЋб—«ћъµƒє§“µЈѕ“Їќ™‘≠Ѕѕ…ъ≤ъ—хїѓћъµƒє§“’»зѕ¬(≤њЈ÷≤ў„чЇЌћхЉю¬‘)£Ї
Ґсі”Јѕ“Ї÷–ћбіњ≤ҐљбЊІ≥цFeSO4°§7H2O£ї
ҐтљЂFeSO4°§7H2O≈д÷∆≥…»№“Ї£ї
ҐуFeSO4»№“Ї”л…‘єэЅњµƒNH4HCO3»№“ЇїмЇѕ£ђµ√µљЇђFeCO3µƒ„«“Ї£ї
ҐфљЂ„«“Їєэ¬Ћ£ђ”√90°ж»»ЋЃѕіµ”≥Ѕµн£ђЄ…‘пЇуµ√µљFeCO3єћће£ї
Ґхм—…’FeCO3£ђµ√µљFe2O3єћће°£
“—÷™£ЇNH4HCO3‘Џ»»ЋЃ÷–Ј÷љв°£
(1)Ґс÷–£ђ“™Љ”„гЅњµƒћъ–Љ≥э»•Јѕ“Ї÷–µƒFe3+£ђЄ√Јі”¶µƒјл„”Јљ≥ћ љ «_______________°£
(2)Ґт÷–£ђ–иЉ”“їґ®ЅњЅтЋб£Ѓ‘Ћ”√їѓ—І∆љЇв‘≠јнЉт цЅтЋбµƒ„ч”√____________________°£
(3)Ґу÷–£ђ…ъ≥…FeCO3µƒјл„”Јљ≥ћ љ «_________________£ђ»фFeCO3„«“Ї≥§ ±Љд±©¬ґ‘Џњ’∆ш÷–£ђїб”–≤њЈ÷єћће±н√ж±дќ™ЇмЇ÷…Ђ£ђЄ√±дїѓµƒїѓ—ІЈљ≥ћ љ «______________________°£
(4)Ґф÷–£ђЌ®єэЉм—йSO42-јі≈–ґѕ≥Ѕµн «Јсѕіµ”Є…Њї£ђЉм—йSO42-µƒ≤ў„ч «_________________________________________________°£
(5)“—÷™м—…’FeCO3µƒїѓ—ІЈљ≥ћ љ «4FeCO3+O2 2Fe2O3+4CO2£ђѕ÷м—…’464.0 kgµƒFeCO3£ђµ√µљ316.8 kg≤ъ∆Ј£ђ»ф≤ъ∆Ј÷–‘”÷ ÷ї”–FeO£ђ‘тЄ√≤ъ∆Ј÷–Fe2O3µƒ÷ Ѕњ «________kg°£(ƒ¶ґы÷ Ѕњ/g°§mol-1£ЇFeCO3 116°°Fe2O3 160°°FeO 72)
2Fe2O3+4CO2£ђѕ÷м—…’464.0 kgµƒFeCO3£ђµ√µљ316.8 kg≤ъ∆Ј£ђ»ф≤ъ∆Ј÷–‘”÷ ÷ї”–FeO£ђ‘тЄ√≤ъ∆Ј÷–Fe2O3µƒ÷ Ѕњ «________kg°£(ƒ¶ґы÷ Ѕњ/g°§mol-1£ЇFeCO3 116°°Fe2O3 160°°FeO 72)
Ґсі”Јѕ“Ї÷–ћбіњ≤ҐљбЊІ≥цFeSO4°§7H2O£ї
ҐтљЂFeSO4°§7H2O≈д÷∆≥…»№“Ї£ї
ҐуFeSO4»№“Ї”л…‘єэЅњµƒNH4HCO3»№“ЇїмЇѕ£ђµ√µљЇђFeCO3µƒ„«“Ї£ї
ҐфљЂ„«“Їєэ¬Ћ£ђ”√90°ж»»ЋЃѕіµ”≥Ѕµн£ђЄ…‘пЇуµ√µљFeCO3єћће£ї
Ґхм—…’FeCO3£ђµ√µљFe2O3єћће°£
“—÷™£ЇNH4HCO3‘Џ»»ЋЃ÷–Ј÷љв°£
(1)Ґс÷–£ђ“™Љ”„гЅњµƒћъ–Љ≥э»•Јѕ“Ї÷–µƒFe3+£ђЄ√Јі”¶µƒјл„”Јљ≥ћ љ «_______________°£
(2)Ґт÷–£ђ–иЉ”“їґ®ЅњЅтЋб£Ѓ‘Ћ”√їѓ—І∆љЇв‘≠јнЉт цЅтЋбµƒ„ч”√____________________°£
(3)Ґу÷–£ђ…ъ≥…FeCO3µƒјл„”Јљ≥ћ љ «_________________£ђ»фFeCO3„«“Ї≥§ ±Љд±©¬ґ‘Џњ’∆ш÷–£ђїб”–≤њЈ÷єћће±н√ж±дќ™ЇмЇ÷…Ђ£ђЄ√±дїѓµƒїѓ—ІЈљ≥ћ љ «______________________°£
(4)Ґф÷–£ђЌ®єэЉм—йSO42-јі≈–ґѕ≥Ѕµн «Јсѕіµ”Є…Њї£ђЉм—йSO42-µƒ≤ў„ч «_________________________________________________°£
(5)“—÷™м—…’FeCO3µƒїѓ—ІЈљ≥ћ љ «4FeCO3+O2
 2Fe2O3+4CO2£ђѕ÷м—…’464.0 kgµƒFeCO3£ђµ√µљ316.8 kg≤ъ∆Ј£ђ»ф≤ъ∆Ј÷–‘”÷ ÷ї”–FeO£ђ‘тЄ√≤ъ∆Ј÷–Fe2O3µƒ÷ Ѕњ «________kg°£(ƒ¶ґы÷ Ѕњ/g°§mol-1£ЇFeCO3 116°°Fe2O3 160°°FeO 72)
2Fe2O3+4CO2£ђѕ÷м—…’464.0 kgµƒFeCO3£ђµ√µљ316.8 kg≤ъ∆Ј£ђ»ф≤ъ∆Ј÷–‘”÷ ÷ї”–FeO£ђ‘тЄ√≤ъ∆Ј÷–Fe2O3µƒ÷ Ѕњ «________kg°£(ƒ¶ґы÷ Ѕњ/g°§mol-1£ЇFeCO3 116°°Fe2O3 160°°FeO 72) (1)Fe+2Fe3+===3Fe2+
(2)Љ”»лЅтЋб£ђH+≈®ґ»‘ціу£ђ єFe2++2H2O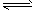 Fe(OH)2+2H+µƒ∆љЇвѕтƒжЈі”¶Јљѕт“∆ґѓ£ђі”ґш“÷÷∆Fe2+µƒЋЃљв
Fe(OH)2+2H+µƒ∆љЇвѕтƒжЈі”¶Јљѕт“∆ґѓ£ђі”ґш“÷÷∆Fe2+µƒЋЃљв
(3)Fe2++2HCO3-===FeCO3°э+CO2°ь+H2O£ї4FeCO3+6H2O+O2===4Fe(OH)3°э+4CO2
(4)»°…ўЅњѕіµ”Їуµƒ»№“ЇЈ≈»л ‘є№÷–£ђµќЉ”—ќЋбЋбїѓµƒBaCl2»№“Ї£ђ»фќё∞„…Ђ≥Ѕµн≤ъ…ъ£ђ‘т≥Ѕµнѕіµ”Є…Њї
(5)288.0
(2)Љ”»лЅтЋб£ђH+≈®ґ»‘ціу£ђ єFe2++2H2O
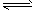 Fe(OH)2+2H+µƒ∆љЇвѕтƒжЈі”¶Јљѕт“∆ґѓ£ђі”ґш“÷÷∆Fe2+µƒЋЃљв
Fe(OH)2+2H+µƒ∆љЇвѕтƒжЈі”¶Јљѕт“∆ґѓ£ђі”ґш“÷÷∆Fe2+µƒЋЃљв (3)Fe2++2HCO3-===FeCO3°э+CO2°ь+H2O£ї4FeCO3+6H2O+O2===4Fe(OH)3°э+4CO2
(4)»°…ўЅњѕіµ”Їуµƒ»№“ЇЈ≈»л ‘є№÷–£ђµќЉ”—ќЋбЋбїѓµƒBaCl2»№“Ї£ђ»фќё∞„…Ђ≥Ѕµн≤ъ…ъ£ђ‘т≥Ѕµнѕіµ”Є…Њї
(5)288.0

ЅЈѕ∞≤бѕµЅ–ір∞Є
ѕаєЎћвƒњ
 £©°£
£©°£
 I і”Јѕ“Ї÷–ћбіњ≤ҐљбЊІі¶FeSO4°§7H2O°£
I і”Јѕ“Ї÷–ћбіњ≤ҐљбЊІі¶FeSO4°§7H2O°£ »№“Ї”л…‘єэЅњµƒ
»№“Ї”л…‘єэЅњµƒ »№“ЇїмЇѕ£ђµ√µљЇђ
»№“ЇїмЇѕ£ђµ√µљЇђ µƒ„«“Ї
µƒ„«“Ї IV љЂ„«“Їєэ¬Ћ£ђ”√90°гC»»ЋЃѕіµ”≥Ѕµн£ђЄ…‘пЇуµ√µљ
IV љЂ„«“Їєэ¬Ћ£ђ”√90°гC»»ЋЃѕіµ”≥Ѕµн£ђЄ…‘пЇуµ√µљ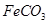 єћће
єћће єћће
єћће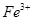 £ђЄ√Јі”¶µƒјл„”Јљ≥ћ љ «
£ђЄ√Јі”¶µƒјл„”Јљ≥ћ љ «
 јі≈–ґѕ≥Ѕµн «Јсѕіµ”Є…Њї°£Љм—й
јі≈–ґѕ≥Ѕµн «Јсѕіµ”Є…Њї°£Љм—й “—÷™м—…’
“—÷™м—…’ £ђѕ÷м—…’464.0kgµƒ
£ђѕ÷м—…’464.0kgµƒ £ђ‘тЄ√≤ъ∆Ј÷–
£ђ‘тЄ√≤ъ∆Ј÷– µƒ÷ Ѕњ «
kg£®ƒ¶ґы÷ Ѕњ/g°§
µƒ÷ Ѕњ «
kg£®ƒ¶ґы÷ Ѕњ/g°§ £ї
£ї £©
£©