题目内容
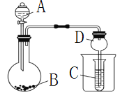
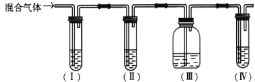
【题目】某化学实验室产生的废液中的阳离子只可能含有Na+、NH4+、Ba2+、Cu2+、Al3+、Fe2+、Fe3+中的某几种,实验室设计了下述方案对废液进行处理,以回收金属,保护环境。
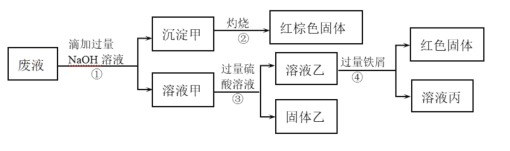
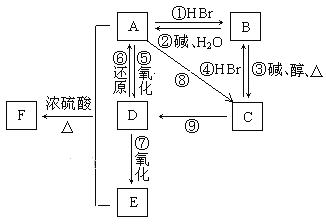
已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解。下列说法中正确的是
A.根据步骤①的现象,说明废液中一定含有Al3+
B.由步骤②中红棕色固体可知,废液中一定存在Fe3+
C.沉淀甲中可能含有Al(OH)3
D.该废液中一定含有NH4+、Ba2+、Cu2+、Fe2+和Fe3+至少存在一种
【答案】D
【解析】
沉淀甲灼烧后为红棕色固体,该红棕色固体为Fe2O3,则沉淀甲可能为Fe(OH)2或Fe(OH)3,说明废液中可能含有Fe2+或Fe3+;溶液甲中加入过量硫酸溶液,产生固体乙,则固体乙为BaSO4,说明废液中一定含有Ba2+;溶液乙中加入过量铁屑,产生红色固体,该红色固体为Cu,说明废液中一定含有Cu2+,以此解答该题。
A. 由步骤④可知,废液中一定含有Cu2+,而沉淀甲中没有Cu(OH)2,说明加入NaOH溶液后,Cu元素以离子形式存在于溶液甲中,则废液中一定含有NH4+,Cu元素以[Cu(NH3)4]2+形式存在于溶液甲中,因此步骤①沉淀部分溶解,不能说明废液中一定含有Al3+,A错误;
B. 废液中加入NaOH溶液后形成沉淀甲,将该沉淀灼烧,得到红棕色固体,则该红棕色固体为Fe2O3,沉淀甲可能为Fe(OH)2或Fe(OH)3,说明废液中可能含有Fe2+或Fe3+,B错误;
C. 由于步骤①中加入过量NaOH溶液,因此沉淀甲中肯定没有Al(OH)3沉淀,C错误;
D. 溶液乙中加入过量铁屑,得到红色固体,该固体为Cu,说明溶液乙中含有Cu2+,向原废液中滴加过量NaOH溶液,Cu元素以离子形式存在于溶液甲中,则废液中一定含有NH4+,Cu元素以[Cu(NH3)4]2+形式存在于溶液甲中,所以废液中一定含有NH4+、Cu2+、Ba2+,可能含有Fe2+或Fe3+中的一种,D正确;
故合理选项是D。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:

相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________,检验生成离子试剂___________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间,除铝的离子反应方程式是__________。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)氧化中除了添加适量MnO2还可以用H2O2来氧化,写出该离子反应_______________。
(6)写出“沉锰”的离子方程式_______________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
(8)写出Fe2+和HNO3的离子反应__________。