题目内容
16.某种物质的结构简式如图,下列描述中不正确的是( )
| A. | 分子式为C9H12 | |
| B. | 1mol此分子在一定条件下最多能与4 molH2发生反应 | |
| C. | 所有碳原子都在同一平面上 | |
| D. | 此物质能被酸性KMnO4溶液氧化 |
分析 由结构可知分子式,分子中含碳碳双键,中间的C为四面体构型,结合烯烃的性质来解答.
解答 解:A.由结构可知分子式为C9H12,故A正确;
B.含4个碳碳双键,则1mol此分子在一定条件下最多能与4 molH2发生反应,故B正确;
C.中间的C为四面体构型,所有碳原子不可能共面,故C错误;
D.含碳碳双键,能被酸性KMnO4溶液氧化,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意甲烷结构及烯烃的性质,题目难度不大.

练习册系列答案
相关题目
18.X、Y、Z、W、R为原子序数依次增大的五种短周期主族元素,X在自然界中形成化合物的种类数最多,Z的一种同素异形体具有杀菌、消毒能力,W的简单离子半径是同周期元素简单离子中最小的,H2在R单质中燃烧产生苍白色火焰.下列有关说法正确的是( )
| A. | 原子半径从大到小为R W Z Y X | |
| B. | 电解熔融状态下W和R形成的化合物可得到单质W | |
| C. | 0.1mol/L的Y的氧化物对应水化物的pH=1 | |
| D. | X、Y、Z的气态氢化物稳定性依次增强,沸点依次升高 |
4.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 18 g D2O和18 g H2O中含有的质子数均为10NA | |
| B. | 50 mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为3NA |
11.以NA 表示阿伏加德罗常数,下列说法正确的是( )
| A. | 12 g石墨中含有C-C键的个数为3NA | |
| B. | 7.8g Na2O2晶体中含有阴阳离子总数为0.4NA | |
| C. | 1 mol SiO2晶体中含有4NASi-O键 | |
| D. | 1.4 g乙烯(C2H4)和丙烯(C3H6)的混合物中含碳氢键数为0.1 NA |
1.1mol己烯雌酚进行4个实验,下列关于其说法正确的是( )


| A. | 反应①生成18mol CO2 | B. | 反应②生成2mol CO2 | ||
| C. | 反应③消耗6mol溴单质 | D. | 反应④脱去2mol水 |
8.下列说法正确的是( )
| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 熔融状态下能导电的物质一定是离子化合物 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 完全由非金属元素形成的化合物中可能含有离子键 |
5. 化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
 化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A. | D点溶液的pH=11.25 | |
| B. | B点溶液中存在 c(H+ )-c(OH- )=c(NO2- )-c(HNO2) | |
| C. | C点时,加入NaOH溶液的体积为20 mL | |
| D. | 25℃时,HNO2的电离常数Ka=1.0×10-55 |
6. 国家食品药品监督管理总局批准了抗H7N9流感药帕拉米韦氯化钠注射液,其结构如图所示.下列关于帕拉米韦的说法正确的是( )
国家食品药品监督管理总局批准了抗H7N9流感药帕拉米韦氯化钠注射液,其结构如图所示.下列关于帕拉米韦的说法正确的是( )
 国家食品药品监督管理总局批准了抗H7N9流感药帕拉米韦氯化钠注射液,其结构如图所示.下列关于帕拉米韦的说法正确的是( )
国家食品药品监督管理总局批准了抗H7N9流感药帕拉米韦氯化钠注射液,其结构如图所示.下列关于帕拉米韦的说法正确的是( )| A. | 帕拉米韦的分子式为C15H27N4O4 | |
| B. | 1 mol帕拉米韦最多可以与3 mol NaOH发生反应 | |
| C. | 帕拉米韦分子中有6个手性碳原子 | |
| D. | 帕拉米韦能发生取代、消去和氧化反应 |
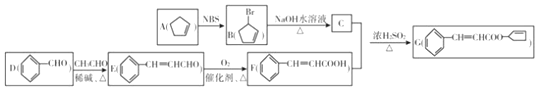
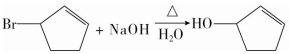 ,其反应类型为取代反应(或水解反应).
,其反应类型为取代反应(或水解反应).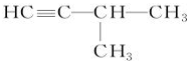 .
.