题目内容
向容积为2L 的密闭容器中充入2mol A 气体和1mol B气体,在一定条件下发生如下反应:2A(g)+B(g)?3C(g);经2s 后反应达平衡,测得C气体的浓度为0.6mol/L.下列说法中不正确的是( )
| A、用A的浓度变化表示的该反应平均速率为0.2 mol/(L?s) | B、平衡时A与B的转化率相等 | C、平衡时B的浓度为0.2 mol/L | D、其它条件不变,向容器中再加入1 mol C,达到新平衡时,C的体积分数不变 |
分析:依据化学平衡三段式列式计算,经2s 后反应达平衡,测得C气体的浓度为0.6mol/L.生成C物质的量=0.6mol/L×2L=1.2mol;
2A(g)+B(g)?3C(g);
起始量(mol) 2 1 0
变化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
A、依据反应速率概念计算得到;
B、计算AB的转化率比较;
C、依据浓度概念计算得到;
D、反应前后是气体体积不变的反应,加入C最后达到相同的平衡状态;
2A(g)+B(g)?3C(g);
起始量(mol) 2 1 0
变化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
A、依据反应速率概念计算得到;
B、计算AB的转化率比较;
C、依据浓度概念计算得到;
D、反应前后是气体体积不变的反应,加入C最后达到相同的平衡状态;
解答:解:依据化学平衡三段式列式计算,经2s 后反应达平衡,测得C气体的浓度为0.6mol/L.生成C物质的量=0.6mol/L×2L=1.2mol;
2A(g)+B(g)?3C(g);
起始量(mol) 2 1 0
变化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
A、用A的浓度变化表示的该反应平均速率=
=0.2 mol/(L?s),故A正确;
B、计算AB的转化率比较,αA=
×100%=40%,αB=
×100%=40%,所以转化率相同,故B正确;
C、依据浓度概念计算得到平衡时B的浓度
=0.3 mol/L,故C错误;
D、反应前后是气体体积不变的反应,加入C相当于增大容器中压强,平衡后达到相同的平衡状态,C的体积分数不变,故D正确;
故选C.
2A(g)+B(g)?3C(g);
起始量(mol) 2 1 0
变化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
A、用A的浓度变化表示的该反应平均速率=
| ||
| 2s |
B、计算AB的转化率比较,αA=
| 0.8mol |
| 2mol |
| 0.4mol |
| 1mol |
C、依据浓度概念计算得到平衡时B的浓度
| 0.6mol |
| 2L |
D、反应前后是气体体积不变的反应,加入C相当于增大容器中压强,平衡后达到相同的平衡状态,C的体积分数不变,故D正确;
故选C.
点评:本题考查了化学平衡三段式计算应用,主要是我在浓度,转化率,反应速率概念的分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196kJ?moL-1,一段时间后达平衡,反应过程中测定的部分数据见下表:
下列说法不正确的是( )
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
| A、反应在前5min的平均速率为v(SO2)=0.08mol?L-1 min-1 |
| B、保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v(正)>v(逆) |
| C、保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收78.4kJ的热量 |
| D、相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40% |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t2>t1),下列说法中正确的是( )
反应过程中测定的部分数据见下表(表中t2>t1),下列说法中正确的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(CO2)=
| ||
| B、到t1 min时,反应未达平衡状态 | ||
| C、保持700℃不变,向平衡体系中再通入0.60molCO和0.30 molH20,达到新平衡时与原平 衡相比,C0转化率增大,H2的体积分数增大 | ||
| D、温度升至800℃时,上述反应的平衡常数为0.64,则正反应为放热反应 |
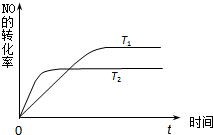
 汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.
汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.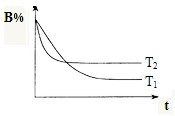 在t℃时,向容积为2L的密闭容器甲中加入1mol A气体、3mol B气体及少量固体催化剂,发生下列反应:A(g)+3B(g)?2C(g);△H<0,10min后各物质的浓度不再变化,测得气体C的体积分数为25%.请填空:
在t℃时,向容积为2L的密闭容器甲中加入1mol A气体、3mol B气体及少量固体催化剂,发生下列反应:A(g)+3B(g)?2C(g);△H<0,10min后各物质的浓度不再变化,测得气体C的体积分数为25%.请填空: