题目内容
【题目】如图所示的实验装置中,A、F分别为NH3和Cl2的发生装置. 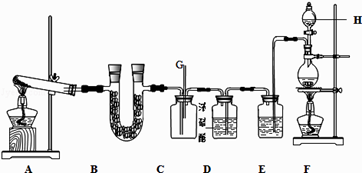
请回答下列问题:
(1)装置F中发生反应的离子方程式为 .
(2)甲、乙两同学分别采用下列两种方案制取C12:甲:用含HCl 146g的浓盐酸与足量的MnO2反应.乙:用87g MnO2与足量浓盐酸反应.则所得氯气(填字母). a.甲比乙多b.乙比甲多c.一样多
(3)仪器H的名称是(填名称),装置E的作用是 .
(4)装置C的导管G处逸出的尾气中可能含有黄绿色的有毒气体,可用进行尾气处理(填选用试剂的名称).
【答案】
(1)MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)b
(3)分液漏斗;除去挥发出的氯化氢
(4)氢氧化钠
【解析】解:(1)装置F用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O, 故答案为:MnO2+4H++2Cl﹣
Mn2++Cl2↑+2H2O, 故答案为:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;(2)根据方程式MnO2+4HCl(浓)
Mn2++Cl2↑+2H2O;(2)根据方程式MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,可知,
MnCl2+Cl2↑+2H2O,可知,
甲:HCl的物质的量为 ![]() =4mol,但随着反应的进行,当为稀盐酸时反应停止,生成的氯气的物质的量小于1mol,
=4mol,但随着反应的进行,当为稀盐酸时反应停止,生成的氯气的物质的量小于1mol,
乙:MnO2的物质的量为 ![]() =1mol,当1molMnO2完全反应时,生成1mol氯气,
=1mol,当1molMnO2完全反应时,生成1mol氯气,
所以乙生成氯气多,
故答案为:b;(3)仪器H具有球形特征,且带有玻璃活塞,名称为分液漏斗,氯气在饱和食盐水中溶解度较小,氯化氢易溶于其中,所以装置E的作用是除去挥发出的氯化氢,
故答案为:分液漏斗;除去挥发出的氯化氢;(4)黄绿色的有毒气体为氯气,氯气是酸性气体,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可以用氢氧化钠来进行尾气处理,
故答案为:氢氧化钠.
由实验装置可知,A、F为为NH3和Cl2的发生装置,A中氨气与碱石灰可制取氨气,B中碱石灰干燥氨气,C为纯净、干燥的氯气与氨气反应的装置,发生8NH3+3Cl2═6NH4Cl+N2 , F中发生MnO2+4HCl ![]() MnCl2+Cl2↑+2H2O,E中饱和食盐水除去HCl,D中浓硫酸干燥氯气,以此来解答.(1)装置F实验室用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水;(2)稀盐酸还原性较弱,不能与二氧化锰发生氧化还原反应生成氯气;(3)根据常见仪器的名称分析,E中用饱和食盐水除去HCl;(4)氯气能够与氢氧化钠溶于反应,据此确定尾气处理的方法.
MnCl2+Cl2↑+2H2O,E中饱和食盐水除去HCl,D中浓硫酸干燥氯气,以此来解答.(1)装置F实验室用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水;(2)稀盐酸还原性较弱,不能与二氧化锰发生氧化还原反应生成氯气;(3)根据常见仪器的名称分析,E中用饱和食盐水除去HCl;(4)氯气能够与氢氧化钠溶于反应,据此确定尾气处理的方法.

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】A同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但他在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体.
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
[提出问题]为什么会生成淡黄色固体?
[查阅资料]该同学查阅资料,记录了右
表中几种物质的颜色:
(1)其他同学认为不必查阅氯化镁的颜色,理由是 ;
(2)[提出猜想]分析资料,A同学认为淡黄色固体可能是由镁与空气中的 反应生成的;
(3)[实验探究]该同学设计实验证实了自己的猜想,他的方案可能是 将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体 ;
(4)[实验结论]根据该同学的实验结果,写出镁条在空气中燃烧时发生的两个反应的化学方程式: 、 ;
(5)[反思与评价]通过上述实验,你对燃烧有什么新的认识? .
【题目】下表为元素周期表的一部分,用化学用语回答下列问题:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为________________________________。
(2)②和③气态氢化物稳定性的大小顺序:___________(填化学式)。
(3)③⑧⑩的最高价含氧酸的酸性最强的是__________(填化学式)。
(4)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是________(填化学式),它属于________(填“共价化合物”或“离子化合物”)。
(5)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为________。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是________(填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性