题目内容
【题目】已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
![]()
起始物质的量浓度/![]() :1.5 1 0
:1.5 1 0
2s末物质的量浓度/![]() :0.9 0.8 0.4
:0.9 0.8 0.4
请回答下列问题。
①该可逆反应的化学方程式可表示为______。
②用物质B来表示![]() 的平均反应速率为______。
的平均反应速率为______。
③从反应开始到2s末,A的转化率为______。
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是______(填序号)
A.![]()
B.容器内气体的总压强保持不变
C容器内气体的密度不变
D.![]()
E.容器内气体C的物质的量分数保持不变
【答案】![]()
![]()
![]() BE
BE
【解析】
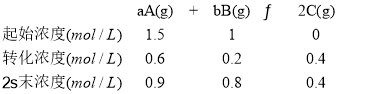
①浓度变化量之比等于对应物质的化学计量数之比,所以![]() ,因
,因![]() ,则
,则![]() ,
,![]() ,所以化学方程式为
,所以化学方程式为![]() 。
。
②![]() 用物质B来表示的反应速率为0.2mol/L÷2s=
用物质B来表示的反应速率为0.2mol/L÷2s=![]() 。
。
③从反应开始到2s末,A物质的转化率![]() 。
。
④A.![]() ,正逆反应速率不相等,A项错误;
,正逆反应速率不相等,A项错误;
B.容器内气体的总压强保持不变,说明气体的物质的量不变,反应达到平衡状态,B项正确;
C.气体质量和容器容积始终不变,容器内气体的密度始终不变,C项错误;
D.只要反应发生,始终有![]() ,D项错误;
,D项错误;
E.容器内气体C的物质的量分数保持不变,说明各组分的物质的量不变,反应达到平衡状态,E项正确。
答案选BE。

【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
【题目】汽车尾气中含有CO、NO等有害气体。
(1)通过NO传感器可监测汽车尾气中NO的含量其工作原理如图所示。已知:![]() 可在固体电解质中自由移动。
可在固体电解质中自由移动。
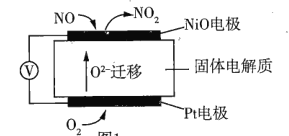
①NO电极上发生的是______(填“氧化”或“还原”)反应。
②外电路中,电子是从______(填“NO”或Pt”)电极流出。
③Pt电极上的电极反应式为______。
(2)一种新型催化剂用于NO和CO的反应:![]() 。已知增大催化剂的比表面积可提高该反应的速率,为了验证温度、催化剂的比表面积对化学反应速率的影响,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应的速率,为了验证温度、催化剂的比表面积对化学反应速率的影响,某同学设计了三组实验,如表所示。
实验编号 |
| NO初始浓度/( | CO初始浓度/( | 催化剂的比表面积( |
Ⅰ | 280 |
|
| 82 |
Ⅱ | 280 |
|
| 124 |
Ⅲ | 350 | a |
| 82 |
①表中a=______。
②能验证温度对化学反应速率影响的是实验______(填实验序号)。
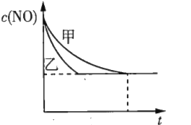
③实验I和实验Ⅱ中,NO的物质的量浓度![]() 随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线______(填“甲”或“乙”)。
随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线______(填“甲”或“乙”)。
(3)在容积固定的绝热容器中发生反应![]() ,不能说明该反应已达到平衡状态的是______(填序号)。
,不能说明该反应已达到平衡状态的是______(填序号)。
A.容器内温度不再变化 B.容器内的气体压强保持不变
C.![]() D.容器内混合气体的密度保持不变
D.容器内混合气体的密度保持不变