题目内容
17.反应4NH3+5O2?4NO+6H2O,在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为( )| A. | v (O2)=0.0016mol/(L•s) | B. | v (NO)=0.08mol/(L•s) | ||
| C. | v (NH3)=0.01mol/(L•s) | D. | v (H2O)=0.003mol/(L•s) |
分析 在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,根据v=$\frac{\frac{△n}{V}}{△t}$计算出用NO表示的反应速率,然后利用反应速率与计量数成正比进行计算.
解答 解:在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,根据v(NO)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.3mol}{5L}}{30s}$=0.002mol/(L•s),
A.v (O2)=$\frac{5}{4}$v(NO)=0.0025mol/(L•s),故A错误;
B.v(NO)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.3mol}{5L}}{30s}$=0.002mol/(L•s),故B错误;
C.v (NH3)=v(NO)=0.002mol/(L•s),故C错误;
D.v(H2O)=$\frac{6}{4}$v(NO)=0.003mol/(L•s),故D正确;
故选D.
点评 本题考查了化学反应速率的计算,题目难度不大,明确化学反应速率与化学计量数的关系为解答关键,注意掌握化学反应速率的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
7.足量的SO2气体通入下列溶液中,不会变成无色溶液的是( )
| A. | 紫色石蕊溶液 | B. | 溴水 | ||
| C. | 酸性高锰酸钾溶液 | D. | 品红溶液 |
8.在标准状况下,0.5mol二氧化碳的体积约是( )
| A. | 0.5L | B. | 22.4L | C. | 11.2L | D. | 44.8L |
12.互为同分异构体的是( )
| A. | 168O与188O | B. | CH4与C2H6 | C. | 正丁烷与异丁烷 | D. | 红磷与白磷 |
2.如表表格中各项分类都正确的一组是( )
类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 生理盐水 | 明矾 | 液态KNO3 | 蔗糖 |
| B | CaO | 海 水 | 铜 | 乙醇 |
| C | 胆矾 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
6.菲的结构简式如图,若菲分子中有1个H原子被Cl原子取代,则所得一氯取代产物有( )
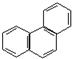

| A. | 4种 | B. | 14种 | C. | 10种 | D. | 5种 |
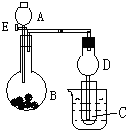 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中:



