题目内容
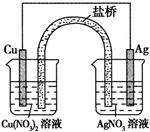
如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)

- A.该原电池的总反应式为2Fe3++Cu=2Fe2++Cu2+
- B.该电池工作时,Cu2+在电极上得到电子,发生还原反应
- C.该电池工作时,氯化铜溶液中氯离子浓度增大
- D.电池工作过程中,电子由铜电极经过电流表流向石墨电极
B
试题分析:A、根据原电池的结构示意图可知该原电池的总反应式为2Fe3++Cu=2Fe2++Cu2+,正确;B、由电池反应分析知Fe3+在电极上得到电子,发生还原反应,错误;C、该电池工作时Cu—2e—=Cu2+,Cu2+进入氯化铜溶液中,盐桥中氯离子进入氯化铜溶液中而使氯离子浓度增大,正确;D、铜电极作负极,石墨电极做正极,电子由正极经过电流表流向负极,正确。
考点:考查原电池的基本原理。
试题分析:A、根据原电池的结构示意图可知该原电池的总反应式为2Fe3++Cu=2Fe2++Cu2+,正确;B、由电池反应分析知Fe3+在电极上得到电子,发生还原反应,错误;C、该电池工作时Cu—2e—=Cu2+,Cu2+进入氯化铜溶液中,盐桥中氯离子进入氯化铜溶液中而使氯离子浓度增大,正确;D、铜电极作负极,石墨电极做正极,电子由正极经过电流表流向负极,正确。
考点:考查原电池的基本原理。

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
 (1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是