题目内容
322g Na2SO4?10H2O的物质的量是________ mol,其中所含的Na+的物质的量是________ mol,SO42-的物质的量是________ mol,所含H2O分子的数目是________个;将322gNa2SO4?10H2O溶于水配成2L溶液,其物质的量浓度是________mol/L.
1 2 1 6.02×1024 0.5
分析:根据n= 来计算一定质量的物质的物质的量,根据Na2SO4?10H2O的构成情况分析各种微粒的多少,据c=
来计算一定质量的物质的物质的量,根据Na2SO4?10H2O的构成情况分析各种微粒的多少,据c= 来计算物质的量浓度.
来计算物质的量浓度.
解答:322g Na2SO4?10H2O的物质的量n= =
=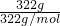 =1mol,钠离子的物质的量是Na2SO4?10H2O的物质的量的2倍,所以其中所含的Na+的物质的量是2mol,硫酸根离子的物质的量和
=1mol,钠离子的物质的量是Na2SO4?10H2O的物质的量的2倍,所以其中所含的Na+的物质的量是2mol,硫酸根离子的物质的量和
Na2SO4?10H2O的物质的量相等,即为1mol,含有H2O分子的物质的量是Na2SO4?10H2O的物质的量的10倍,数目是10NA,即6.02×1024个,将322gNa2SO4?10H2O溶于水配成2L溶液,其物质的量浓度c= =
=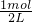 =0.5mol/L.
=0.5mol/L.
故答案为:1;2;1;6.02×1024;0.5.
点评:本题是一道关于物质的量的计算题,可以根据所学知识来回答,难度不大.
分析:根据n=
 来计算一定质量的物质的物质的量,根据Na2SO4?10H2O的构成情况分析各种微粒的多少,据c=
来计算一定质量的物质的物质的量,根据Na2SO4?10H2O的构成情况分析各种微粒的多少,据c= 来计算物质的量浓度.
来计算物质的量浓度.解答:322g Na2SO4?10H2O的物质的量n=
 =
=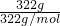 =1mol,钠离子的物质的量是Na2SO4?10H2O的物质的量的2倍,所以其中所含的Na+的物质的量是2mol,硫酸根离子的物质的量和
=1mol,钠离子的物质的量是Na2SO4?10H2O的物质的量的2倍,所以其中所含的Na+的物质的量是2mol,硫酸根离子的物质的量和Na2SO4?10H2O的物质的量相等,即为1mol,含有H2O分子的物质的量是Na2SO4?10H2O的物质的量的10倍,数目是10NA,即6.02×1024个,将322gNa2SO4?10H2O溶于水配成2L溶液,其物质的量浓度c=
 =
=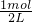 =0.5mol/L.
=0.5mol/L.故答案为:1;2;1;6.02×1024;0.5.
点评:本题是一道关于物质的量的计算题,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
下列关于1mol/L Na2SO4溶液的说法正确的是.( )
| A、溶液中含有1mol Na2SO4 | B、1mol Na2SO4溶于1L蒸馏水中 | C、将322g Na2SO4?10H2O溶于少量水后再稀释到1000mL | D、将322g Na2SO4?10H2O溶于少量水后再稀释到500mL |