题目内容
某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、[Al(OH)4]-、S2-、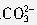 、
、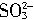 、
、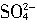 。现取该溶液进行如下实验:①无色溶液中加入过量氢溴酸溶液并加热,得到气体甲、淡黄色沉淀甲和溶液甲;②溶液甲中加入过量NH4HCO3溶液,得到气体乙、白色沉淀乙和溶液乙;③溶液乙中加入过量Ba(OH)2溶液并加热,得到气体丙、白色沉淀丙和溶液丙。请回答下列问题:
。现取该溶液进行如下实验:①无色溶液中加入过量氢溴酸溶液并加热,得到气体甲、淡黄色沉淀甲和溶液甲;②溶液甲中加入过量NH4HCO3溶液,得到气体乙、白色沉淀乙和溶液乙;③溶液乙中加入过量Ba(OH)2溶液并加热,得到气体丙、白色沉淀丙和溶液丙。请回答下列问题:(1)生成沉淀甲的离子方程式为_____________,由溶液甲生成沉淀乙的离子方程式为____________。
(2)气体甲的成分有哪几种可能,请一一列出:_________________________________________。
(3)综合上述现象,可以肯定存在的离子有___________________。
(1)2S2-+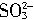 +6H+=3S↓+3H2O;
+6H+=3S↓+3H2O;
Al3++3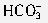 =Al(OH)3↓+3CO2↑
=Al(OH)3↓+3CO2↑
(2)有5种可能:①CO2、②H2S、③H2S和CO2、
④SO2、⑤SO2和CO2
(3)Na+、[Al(OH)4]-、S2-、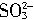
【试题分析】

练习册系列答案
相关题目
