题目内容
【题目】在不同条件下,![]() 的密闭容器中发生如下反应
的密闭容器中发生如下反应![]() 。已知Y、Z的起始浓度为0,X的浓度
。已知Y、Z的起始浓度为0,X的浓度![]() 随反应时间
随反应时间![]() 变化的情况如下表:
变化的情况如下表:

下列说法不正确的是![]()
![]()
A.![]()
B.与实验1比较,实验2反应速率加快,原因可能是加入了合适的催化剂或增大体系压强
C.在实验3中,![]() 时间段内反应体系总共减少的X的物质的量为
时间段内反应体系总共减少的X的物质的量为![]()
D.若![]() ,则可说明
,则可说明![]() 的
的![]()
【答案】B
【解析】
A.实验2与实验1达到的平衡状态相同,则![]() ,实验3达到平衡X的浓度大于实验1,温度相同,说明X的起始浓度
,实验3达到平衡X的浓度大于实验1,温度相同,说明X的起始浓度![]()
![]() ,故A正确;
,故A正确;
B.实验2与实验1达到的平衡状态相同,而实验2达平衡用时短,反应速率快可能使用了催化剂;若增大体系压强,平衡虽然不移动,各个物质的浓度会改变,导致实验2与实验1达到的平衡状态不相同,故B错误;
C. ![]()
![]()
![]()
![]()
起始![]()
![]() 0 0
0 0
转化![]()
![]()
![]()
平衡![]()
![]()
![]()
实验1和实验3的温度相同,平衡常数相同,所以 ,
,![]() ,
,![]() 时间段内反应体系总共减少的X的物质的量为
时间段内反应体系总共减少的X的物质的量为![]() ,故 C正确;
,故 C正确;
D.若![]() ,根据
,根据![]() ,温度升高,平衡常数增大,说明正反应是吸热反应,逆反应
,温度升高,平衡常数增大,说明正反应是吸热反应,逆反应![]() 的
的![]() ,故D正确;
,故D正确;
故答案选B。

【题目】有反应:![]() ,
,![]() 时该反应的平衡常数
时该反应的平衡常数![]() 。
。![]() 时,将一定量的
时,将一定量的![]() 和
和![]() 充入容积为某10L密闭容器发生上述反应,5min时达平衡,
充入容积为某10L密闭容器发生上述反应,5min时达平衡,![]() 只改变了一个条件,10min时再次达平衡,各物质物质的量
只改变了一个条件,10min时再次达平衡,各物质物质的量![]() 变化如下:
变化如下:
0min | 5min | 10min | |
CO |
|
| |
|
|
| |
| 0 |
| |
| 0 |
|
下列说法正确的是![]()
A.![]() 时用
时用![]() 表示的平均反应速率为
表示的平均反应速率为![]()
B.![]() 改变的条件是再加入了
改变的条件是再加入了![]()
![]()
C.![]() 时,若向容器中充入
时,若向容器中充入![]()
![]() 、
、![]()
![]() 、
、![]() 、
、![]() ,达平衡时,
,达平衡时,![]() 的浓度为
的浓度为![]()
D.![]() 时,若向容器中充入
时,若向容器中充入![]()
![]() 、
、![]()
![]() 、
、![]() 、
、![]()
![]() 正
正![]() 逆
逆![]()
【题目】一定温度下,在4个体积均为 1.0 L的恒容密闭容器中反应2SO2(g)+O2 (g)![]() 2SO3(g) 达到平衡。
2SO3(g) 达到平衡。
下列说法正确的是
容器 | 温度/K | 物质的起始浓度/moI/L | 物质的平衡浓度moI/L | O2或SO3平衡转化率 | ||
c(SO2) | c(O2) | c(SO3) | c(SO3) | |||
Ⅰ | 723 | 0.2 | 0.2 | 0 | 0.04 | α1 |
Ⅱ | 723 | 0 | 0.1 | 0.2 | α2 | |
Ⅲ | 723 | 0.4 | 0.4 | 0 | α3 | |
IV | 823 | 0 | 0.1 | 0.2 | α4 | |
A. 达到平衡时, α1+α2=1
B. 达到平衡时,容器中的压强:PⅠ>PIV
C. 达到平衡时,逆反应速率容器IV中比容器Ⅰ中的大
D. 达平衡后,再向容器Ⅰ中充入0.16 mol SO2、0.04 mol SO3,则此时反应向逆反应方向进行
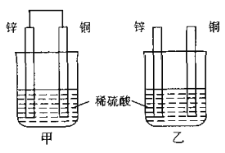
【题目】下图所示的实验,能达到实验目的的是
A | B | C | D |
|
|
片刻后在 Fe 电极附近滴入铁氰化钾溶液 |
|
验证化学能转化为电能 | 证明温度对平衡移动的影响 | 验证 Fe 电极被保护 | 验证AgCl 溶解度大于Ag2S |
A.AB.BC.CD.D