ΧβΡΩΡΎ»ί
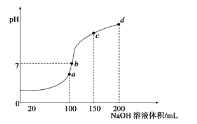
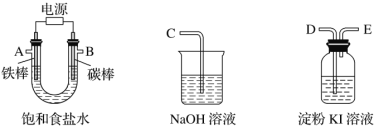
ΓΨΧβΡΩΓΩΘ®1Θ©“‘œ¬Ν–≥ωΒΡ «“Μ–©‘≠Ή”ΒΡ2pΡήΦΕΚΆ3dΡήΦΕ÷–ΒγΉ”≈≈≤ΦΒΡ«ιΩωΘ§ ‘≈–ΕœΡΡ–©ΈΞΖ¥ΝΥ≈ίάϊ‘≠άμ________Θ§ΡΡ–©ΈΞΖ¥ΝΥΚιΧΊΙφ‘ρ________ΓΘ
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
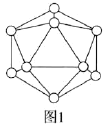
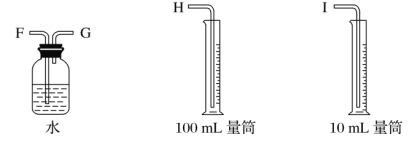
Θ®2Θ©![]() Ω…”Ο”Ύ÷Τ‘λΜπ≤ώΘ§ΤδΖ÷Ή”ΫαΙΙ»γΆΦΥυ ΨΓΘ
Ω…”Ο”Ύ÷Τ‘λΜπ≤ώΘ§ΤδΖ÷Ή”ΫαΙΙ»γΆΦΥυ ΨΓΘ

![]() Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣ________ΓΘ
Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣ________ΓΘ
![]() ΟΩΗω
ΟΩΗω![]() Ζ÷Ή”÷–Κ§”–ΒΡΙ¬ΒγΉ”Ε‘ΒΡ ΐΡΩΈΣ________ΓΘ
Ζ÷Ή”÷–Κ§”–ΒΡΙ¬ΒγΉ”Ε‘ΒΡ ΐΡΩΈΣ________ΓΘ
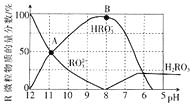
Θ®3Θ©ΩΤ―ßΦ“Κœ≥…ΝΥ“Μ÷÷―τάκΉ”ΓΑ![]() Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘΜ¥ΥΚσ”÷Κœ≥…ΝΥ“Μ÷÷Κ§”–ΓΑ
Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘΜ¥ΥΚσ”÷Κœ≥…ΝΥ“Μ÷÷Κ§”–ΓΑ![]() Γ±ΒΡΜ·―ß ΫΈΣΓΑ
Γ±ΒΡΜ·―ß ΫΈΣΓΑ![]() Γ±ΒΡάκΉ”ΨßΧεΘ§ΤδΒγΉ” ΫΈΣ________ΓΘΖ÷Ή”
Γ±ΒΡάκΉ”ΨßΧεΘ§ΤδΒγΉ” ΫΈΣ________ΓΘΖ÷Ή”![]() ÷–Φϋ”κΦϋ÷°ΦδΒΡΦ–Ϋ«ΈΣ
÷–Φϋ”κΦϋ÷°ΦδΒΡΦ–Ϋ«ΈΣ![]() Θ§≤Δ”–Ε‘≥Τ–‘Θ§Ζ÷Ή”÷–ΟΩΗω‘≠Ή”ΒΡΉνΆβ≤ψΨυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΤδΫαΙΙ ΫΈΣ________________ΓΘ
Θ§≤Δ”–Ε‘≥Τ–‘Θ§Ζ÷Ή”÷–ΟΩΗω‘≠Ή”ΒΡΉνΆβ≤ψΨυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΤδΫαΙΙ ΫΈΣ________________ΓΘ
Θ®4Θ©÷±Ν¥ΕύΝΉΥαΗυ“θάκΉ” «”…ΝΫΗωΜρΝΫΗω“‘…œΝΉ―θΥΡΟφΧεΆ®ΙΐΙ≤”ΟΕΞΫ«―θ‘≠Ή”Ν§Ϋ”Τπά¥ΒΡΘ§»γΆΦΥυ ΨΓΘ‘ρ”…nΗωΝΉ―θΥΡΟφΧε–Έ≥…ΒΡ’βάύΝΉΥαΗυάκΉ”ΒΡΆ® ΫΈΣ________ΓΘ
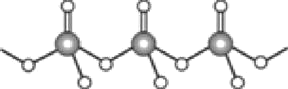
Θ®5Θ©ΧΦΥα―Έ÷–ΒΡ―τάκΉ”≤ΜΆ§Θ§»»Ζ÷ΫβΈ¬Ε»ΨΆ≤ΜΆ§ΓΘœ¬±μΈΣΥΡ÷÷ΧΦΥα―ΈΒΡ»»Ζ÷ΫβΈ¬Ε»ΚΆΫπ τ―τάκΉ”ΑκΨΕ
ΧΦΥα―Έ |
|
|
|
|
»»Ζ÷ΫβΈ¬Ε» | 402 | 900 | 1172 | 1360 |
Ϋπ τ―τάκΉ”ΑκΨΕ | 66 | 99 | 112 | 135 |
ΥφΉ≈Ϋπ τ―τάκΉ”ΑκΨΕΒΡ‘ω¥σΘ§ΧΦΥα―ΈΒΡ»»Ζ÷ΫβΈ¬Ε»÷π≤Ϋ…ΐΗΏΘ§‘≠“ρ «_____________ΓΘ
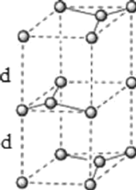
Θ®6Θ© ·ΡΪΒΡΨßΧεΫαΙΙΚΆΨßΑϊΫαΙΙ»γΆΦΥυ ΨΓΘ“―÷Σ ·ΡΪΒΡΟήΕ»ΈΣ![]() Θ§
Θ§![]() ΦϋΒΡΦϋ≥ΛΈΣ
ΦϋΒΡΦϋ≥ΛΈΣ![]() Θ§ΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΈΣ
Θ§ΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΈΣ![]() Θ§‘ρ ·ΡΪΨßΧεΒΡ≤ψΦδΨύΈΣ________cmΓΘ
Θ§‘ρ ·ΡΪΨßΧεΒΡ≤ψΦδΨύΈΣ________cmΓΘ
 ΓΘ
ΓΘ
ΓΨ¥πΑΗΓΩ![]()
![]()
![]()
![]()
![]()
![]()
![]() ΧΦΥα―ΈΖ÷Ϋβ ΒΦ Ιΐ≥Χ «ΨßΧε÷–―τάκΉ”ΫαΚœΧΦΥαΗυάκΉ”÷–―θάκΉ”Θ§ ΙΧΦΥαΗυάκΉ”Ζ÷ΫβΈΣΕΰ―θΜ·ΧΦΒΡΙΐ≥ΧΘ§―τάκΉ”Υυ¥χΒγΚ…œύΆ§ ±Θ§―τάκΉ”ΑκΨΕ‘Ϋ–ΓΘ§ΤδΫαΚœ―θάκΉ”ΡήΝΠ‘Ϋ«ΩΘ§Ε‘”ΠΒΡΧΦΥα―ΈΨΆ‘Ϋ»ί“ΉΖ÷Ϋβ
ΧΦΥα―ΈΖ÷Ϋβ ΒΦ Ιΐ≥Χ «ΨßΧε÷–―τάκΉ”ΫαΚœΧΦΥαΗυάκΉ”÷–―θάκΉ”Θ§ ΙΧΦΥαΗυάκΉ”Ζ÷ΫβΈΣΕΰ―θΜ·ΧΦΒΡΙΐ≥ΧΘ§―τάκΉ”Υυ¥χΒγΚ…œύΆ§ ±Θ§―τάκΉ”ΑκΨΕ‘Ϋ–ΓΘ§ΤδΫαΚœ―θάκΉ”ΡήΝΠ‘Ϋ«ΩΘ§Ε‘”ΠΒΡΧΦΥα―ΈΨΆ‘Ϋ»ί“ΉΖ÷Ϋβ ![]()
ΓΨΫβΈωΓΩ
Θ®1Θ©ΗυΨί≈ίάϊ≤Μœύ»ί‘≠άμΓΔΚιΧΊΙφ‘ρΒΡΡΎ»ίΖ÷ΈωΜΊ¥πΘΜ
Θ®2Θ©![]() Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «
Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «![]() Θ§
Θ§![]() Φϋ ΐ «2ΘΜ
Φϋ ΐ «2ΘΜ
![]() Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «
Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «![]() ΓΔΝΉ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «
ΓΔΝΉ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «![]() ΘΜ
ΘΜ
Θ®3Θ©”…”Ύ―τάκΉ”ΓΑ![]() Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘ§Υυ“‘ΗΟΈΔΝΘ¥χ”–“ΜΗωΒΞΈΜΒΡ’ΐΒγΚ…Θ§ΒγΉ” Ϋ «
Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘ§Υυ“‘ΗΟΈΔΝΘ¥χ”–“ΜΗωΒΞΈΜΒΡ’ΐΒγΚ…Θ§ΒγΉ” Ϋ «![]() Θ§Κ§”–ΓΑ
Θ§Κ§”–ΓΑ![]() Γ±ΒΡΜ·―ß ΫΈΣΓΑ
Γ±ΒΡΜ·―ß ΫΈΣΓΑ![]() Γ±ΒΡάκΉ”ΨßΧεΘ§‘ρΗΟ“θάκΉ” «
Γ±ΒΡάκΉ”ΨßΧεΘ§‘ρΗΟ“θάκΉ” «![]() ΓΘ
ΓΘ
Θ®4Θ©άϊ”ΟΓΑ ΐ―ßΙιΡ…Ζ®Γ±Ζ÷ΈωΆ® ΫΘΜ
Θ®5Θ©ΧΦΥα―ΈΖ÷Ϋβ ΒΦ Ιΐ≥Χ «ΨßΧε÷–―τάκΉ”ΫαΚœΧΦΥαΗυάκΉ”÷–―θάκΉ”Θ§ ΙΧΦΥαΗυάκΉ”Ζ÷ΫβΈΣΕΰ―θΜ·ΧΦΒΡΙΐ≥ΧΘΜ
Θ®6Θ©ΨßΑϊΒΡΗΏΒ»”Ύ≤ψΦδΨύΒΡ2±ΕΓΘ
![]() ≈ίάϊ‘≠άμ÷ΗΒΡ «Ά§“ΜΗω‘≠Ή”ΙλΒάΡΎ≤ΜΩ…Ρή”–ΝΫΗωΉ‘–ΐΖΫœρœύΆ§ΒΡΒγΉ”Θ§“ρ¥ΥΈΞΖ¥≈ίάϊ‘≠άμΒΡ «
≈ίάϊ‘≠άμ÷ΗΒΡ «Ά§“ΜΗω‘≠Ή”ΙλΒάΡΎ≤ΜΩ…Ρή”–ΝΫΗωΉ‘–ΐΖΫœρœύΆ§ΒΡΒγΉ”Θ§“ρ¥ΥΈΞΖ¥≈ίάϊ‘≠άμΒΡ «![]() ΘΜΚιΧΊΙφ‘ρ÷ΗΒΡ «ΒγΉ”ΨΓΩ…ΡήΖ÷’Φ≤ΜΆ§ΙλΒάΘ§«“Ή‘–ΐΖΫœρœύΆ§Θ§“ρ¥ΥΈΞΖ¥ΚιΧΊΙφ‘ρΒΡ «
ΘΜΚιΧΊΙφ‘ρ÷ΗΒΡ «ΒγΉ”ΨΓΩ…ΡήΖ÷’Φ≤ΜΆ§ΙλΒάΘ§«“Ή‘–ΐΖΫœρœύΆ§Θ§“ρ¥ΥΈΞΖ¥ΚιΧΊΙφ‘ρΒΡ «![]() ΘΜ
ΘΜ
Θ®2Θ©![]() Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «
Ζ÷Ή”÷–Νρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐ «![]() Θ§
Θ§![]() Φϋ ΐ «2Θ§‘”Μ·ΙλΒά ΐ «4Θ§Υυ“‘Νρ‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣ
Φϋ ΐ «2Θ§‘”Μ·ΙλΒά ΐ «4Θ§Υυ“‘Νρ‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣ![]() ΘΜ
ΘΜ
![]() ΟΩΗωΝΉ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐΈΣ1Θ§ΟΩΗωΝρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ΈΣ2Θ§Υυ“‘ΟΩΗω
ΟΩΗωΝΉ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ ΐΈΣ1Θ§ΟΩΗωΝρ‘≠Ή”ΒΡΙ¬ΒγΉ”Ε‘ΈΣ2Θ§Υυ“‘ΟΩΗω![]() Ζ÷Ή”÷–Κ§”–ΒΡΙ¬ΒγΉ”Ε‘ΒΡ ΐΡΩΈΣ10ΘΜ
Ζ÷Ή”÷–Κ§”–ΒΡΙ¬ΒγΉ”Ε‘ΒΡ ΐΡΩΈΣ10ΘΜ
![]() ”…”Ύ―τάκΉ”ΓΑ
”…”Ύ―τάκΉ”ΓΑ![]() Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘ§Υυ“‘ΗΟΈΔΝΘ¥χ”–“ΜΗωΒΞΈΜΒΡ’ΐΒγΚ…Θ§ΗΟάκΉ”ΒΡΒγΉ” Ϋ «
Γ±Θ§ΤδΫαΙΙ «Ε‘≥ΤΒΡΘ§5ΗωN≈≈≥…ΓΑVΓ±–ΈΘ§ΟΩΗωNΕΦ¥οΒΫ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§«“Κ§”–2ΗωΒΣΒΣ»ΐΦϋΘ§Υυ“‘ΗΟΈΔΝΘ¥χ”–“ΜΗωΒΞΈΜΒΡ’ΐΒγΚ…Θ§ΗΟάκΉ”ΒΡΒγΉ” Ϋ «![]() Θ§Κ§”–ΓΑ
Θ§Κ§”–ΓΑ![]() Γ±ΒΡΜ·―ß ΫΈΣΓΑ
Γ±ΒΡΜ·―ß ΫΈΣΓΑ![]() Γ±ΒΡάκΉ”ΨßΧεΘ§‘ρΗΟ“θάκΉ” «
Γ±ΒΡάκΉ”ΨßΧεΘ§‘ρΗΟ“θάκΉ” «![]() ΓΘΜ·―ß ΫΈΣΓΑ
ΓΘΜ·―ß ΫΈΣΓΑ![]() Γ±ΒΡάκΉ”ΨßΧεΒΡΒγΉ” ΫΈΣ
Γ±ΒΡάκΉ”ΨßΧεΒΡΒγΉ” ΫΈΣ![]() ΘΜΖ÷Ή”
ΘΜΖ÷Ή”![]() ÷–Φϋ”κΦϋ÷°ΦδΒΡΦ–Ϋ«ΈΣ
÷–Φϋ”κΦϋ÷°ΦδΒΡΦ–Ϋ«ΈΣ![]() Θ§≤Δ”–Ε‘≥Τ–‘Θ§Ζ÷Ή”÷–ΟΩΗω‘≠Ή”ΒΡΉνΆβ≤ψΨυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΤδΫαΙΙ ΫΈΣ
Θ§≤Δ”–Ε‘≥Τ–‘Θ§Ζ÷Ή”÷–ΟΩΗω‘≠Ή”ΒΡΉνΆβ≤ψΨυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΤδΫαΙΙ ΫΈΣ![]() ΘΜ
ΘΜ
![]() ΗυΨίΗχΕ®ΒΡΫαΙΙΘ§”… ΐ―ßΙιΡ…Ζ®Ω…÷ΣΘ§”…nΗωΝΉ―θΥΡΟφΧε–Έ≥…ΒΡ’βάύΝΉΥαΗυάκΉ”ΒΡΆ® ΫΈΣ
ΗυΨίΗχΕ®ΒΡΫαΙΙΘ§”… ΐ―ßΙιΡ…Ζ®Ω…÷ΣΘ§”…nΗωΝΉ―θΥΡΟφΧε–Έ≥…ΒΡ’βάύΝΉΥαΗυάκΉ”ΒΡΆ® ΫΈΣ![]() ΘΜ
ΘΜ
![]() ΥφΉ≈Ϋπ τ―τάκΉ”ΑκΨΕΒΡ‘ω¥σΘ§ΧΦΥα―ΈΒΡ»»Ζ÷ΫβΈ¬Ε»÷π≤Ϋ…ΐΗΏΘ§‘≠“ρ «ΧΦΥα―ΈΖ÷Ϋβ ΒΦ Ιΐ≥Χ «ΨßΧε÷–―τάκΉ”ΫαΚœΧΦΥαΗυάκΉ”÷–―θάκΉ”Θ§ ΙΧΦΥαΗυάκΉ”Ζ÷ΫβΈΣΕΰ―θΜ·ΧΦΒΡΙΐ≥ΧΘ§―τάκΉ”Υυ¥χΒγΚ…œύΆ§ ±Θ§―τάκΉ”ΑκΨΕ‘Ϋ–ΓΘ§ΤδΫαΚœ―θάκΉ”ΡήΝΠ‘Ϋ«ΩΘ§Ε‘”ΠΒΡΧΦΥα―ΈΨΆ‘Ϋ»ί“ΉΖ÷ΫβΘΜ
ΥφΉ≈Ϋπ τ―τάκΉ”ΑκΨΕΒΡ‘ω¥σΘ§ΧΦΥα―ΈΒΡ»»Ζ÷ΫβΈ¬Ε»÷π≤Ϋ…ΐΗΏΘ§‘≠“ρ «ΧΦΥα―ΈΖ÷Ϋβ ΒΦ Ιΐ≥Χ «ΨßΧε÷–―τάκΉ”ΫαΚœΧΦΥαΗυάκΉ”÷–―θάκΉ”Θ§ ΙΧΦΥαΗυάκΉ”Ζ÷ΫβΈΣΕΰ―θΜ·ΧΦΒΡΙΐ≥ΧΘ§―τάκΉ”Υυ¥χΒγΚ…œύΆ§ ±Θ§―τάκΉ”ΑκΨΕ‘Ϋ–ΓΘ§ΤδΫαΚœ―θάκΉ”ΡήΝΠ‘Ϋ«ΩΘ§Ε‘”ΠΒΡΧΦΥα―ΈΨΆ‘Ϋ»ί“ΉΖ÷ΫβΘΜ
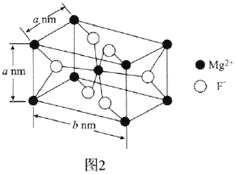
![]() ΗυΨί ·ΡΪΒΡΫαΙΙΖ÷ΈωΩ…÷Σ ·ΡΪΨßΧε÷–Κ§”–ΒΡΧΦ‘≠Ή” ΐΈΣ
ΗυΨί ·ΡΪΒΡΫαΙΙΖ÷ΈωΩ…÷Σ ·ΡΪΨßΧε÷–Κ§”–ΒΡΧΦ‘≠Ή” ΐΈΣ![]() Θ§”÷
Θ§”÷![]() ΦϋΒΡΦϋ≥ΛΈΣrcmΘ§Υυ“‘ΨßΑϊΒΡΒΉΟφΜΐΈΣ
ΦϋΒΡΦϋ≥ΛΈΣrcmΘ§Υυ“‘ΨßΑϊΒΡΒΉΟφΜΐΈΣ![]() Θ§ΗυΨίΨßΑϊΒΡΟήΕ»
Θ§ΗυΨίΨßΑϊΒΡΟήΕ» Θ§ΫβΒΟ
Θ§ΫβΒΟ![]() ΓΘ
ΓΘ

ΓΨΧβΡΩΓΩœϊ≥ΐΒΣ―θΜ·ΈοΓΔΕΰ―θΜ·ΝρΒ»Έο÷ ‘λ≥…ΒΡΈέ»Ψ «ΡΩ«Α―–ΨΩΒΡ÷Ί“ΣΩΈΧβΓΘ
(1)ΙΛ“Β…œ≥Θ”ΟΜν–‘ΧΩΜΙ‘≠“Μ―θΜ·ΒΣΘ§ΤδΖ¥”ΠΈΣΘΚ2NO(g)+C(s) N2(g)+CO2(g)ΓΘœρ»ίΜΐΨυΈΣl LΒΡΦΉΓΔ““ΓΔ±ϊ»ΐΗωΚψ»ίΚψΈ¬»ίΤς÷–Ζ÷±πΦ”»κΉψΝΩΒΡΜν–‘ΧΩΚΆ“ΜΕ®ΝΩΒΡNOΘ§≤βΒΟΗς»ίΤς÷–n(NO)ΥφΖ¥”Π ±ΦδtΒΡ±δΜ·«ιΩω»γœ¬±μΥυ ΨΘΚ
0min | 40min | 80min | 120min | 160min | ||
ΦΉ | TΓφ | 2mol | 1.45 mol | 1 mol | 1 mol | 1 mol |
““ | 400Γφ | 2 mol | 1.5 mol | 1.1 mol | 0.8 mol | 0.8 mol |
±ϊ | 400Γφ | 1 mol | 0.8 mol | 0.65 mol | 0.53 mol | 0.45 mol |
ΦΉ»ίΤςΖ¥”ΠΈ¬Ε»TΓφ______400Γφ(ΧνΓΑ>Γ±ΓΑ<Γ±ΜρΓΑ=Γ±)ΘΜ““»ίΤς÷–Θ§0~40minΡΎΤΫΨυΖ¥”ΠΥΌ¬ v(CO2)=_____________________ΘΜ±ϊ»ίΤς÷–¥οΤΫΚβΚσNOΒΡΈο÷ ΒΡΝΩΈΣ_________molΓΘ
(2)Μν–‘ΧΩΜΙ‘≠NO2ΒΡΖ¥”ΠΈΣΘΚ2NO2(g)+2C(s) N2(g)+2CO2(g)Θ§‘ΎΚψΈ¬ΧθΦΰœ¬Θ§l mol NO2ΚΆΉψΝΩΜν–‘ΧΩΖΔ…ζΗΟΖ¥”ΠΘ§≤βΒΟΤΫΚβ ±NO2ΚΆCO2ΒΡΈο÷ ΒΡΝΩ≈®Ε»”κΤΫΚβΉή―ΙΒΡΙΊœΒ»γΆΦΥυ ΨΘΚ
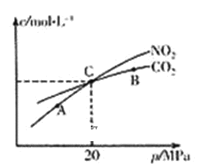
ΔΌAΓΔBΓΔC»ΐΒψ÷–NO2ΒΡΉΣΜ·¬ ΉνΗΏΒΡ «_________Βψ(ΧνΓΑAΓ±ΜρΓΑBΓ±ΜρΓΑCΓ±)ΓΘ
ΔΎΦΤΥψCΒψ ±ΗΟΖ¥”ΠΒΡ―Ι«ΩΤΫΚβ≥Θ ΐKP=_______MPa(Kp «”ΟΤΫΚβΖ÷―Ι¥ζΧφΤΫΚβ≈®Ε»ΦΤΥψΘ§Ζ÷―Ι=Ήή―ΙΓΝΈο÷ ΒΡΝΩΖ÷ ΐ)ΓΘ
(3)»ΦΟΚ―ΧΤχΆ―Νρ≥Θ”Ο»γœ¬ΖΫΖ®ΓΘ
ΖΫΖ®ΔΌΘΚ”Ο…ζΈο÷ »»ΫβΤχ(÷ς“Σ≥…Ζ÷COΓΔCH4ΓΔH2)ΫΪSO2‘ΎΗΏΈ¬œ¬ΜΙ‘≠≥…ΒΞ÷ ΝρΓΘ…φΦΑΒΡ≤ΩΖ÷Ζ¥”Π»γœ¬ΘΚ
2CO(g)+SO2(g)=S(g)+2CO2(g) ΓςH1=8.0 kJΓΛmol-1
2CO(g)+O2(g)=2CO2(g) ΓςH2=Θ≠566.0kJΓΛmol-1
2H2(g)+O2(g)=2H2O(g) ΓςH3=Θ≠483.6 1kJΓΛmol-1
‘ρH2(g)ΜΙ‘≠SO2(g)…ζ≥…S(g)ΚΆH2O(g)ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚ_____________________ΓΘ