题目内容
Cl2与Mg反应,当有0.5 mol Cl2被还原时,共转移电子的物质的量为
- A.1 mol
- B.2 mol
- C.6.02×1023
- D.1.204×1024
A
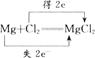 ,当1 mol Cl2参加反应,电子转移数为2 mol,故0.5 mol Cl2被还原时,共转移电子数为1 mol。
,当1 mol Cl2参加反应,电子转移数为2 mol,故0.5 mol Cl2被还原时,共转移电子数为1 mol。
 ,当1 mol Cl2参加反应,电子转移数为2 mol,故0.5 mol Cl2被还原时,共转移电子数为1 mol。
,当1 mol Cl2参加反应,电子转移数为2 mol,故0.5 mol Cl2被还原时,共转移电子数为1 mol。 
练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目