题目内容
20.向铜粉和铁粉中加入过量热的浓硝酸,充分反应后,溶液中大量共存的金属阳离子是( )| A. | Fe2+ | B. | Fe3+ | C. | Fe3+、Cu2+ | D. | Fe2+ Cu2+ |
分析 向铜粉和铁粉中加入过量热的浓硝酸,发生氧化还原反应后溶液中含铁离子、铜离子及硝酸,以此来解答.
解答 解:Cu与硝酸反应生成硝酸铜,溶液中含Cu2+;因硝酸过量,则Fe与硝酸反应生成硝酸铁,则溶液中还含大量的Fe3+,
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,注意硝酸过量,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
10.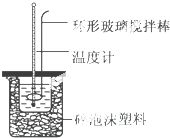 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
完成下列问题
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8 kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”或“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABE.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据| 实验次数 | 起始温度t1/℃ | 终止温 度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8 kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”或“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABE.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.
11.水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
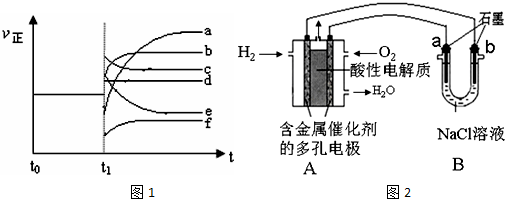
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
(6 )如图2是利用氢氧燃料作电源,用惰性电极电解200ml 1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气4.48L(设电解后溶液体积不变).
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.

C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ①0.6 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ②ν正>ν逆 |
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.
8.下列分子式表示的物质一定是纯净物的是( )
| A. | C4H10 | B. | CH2Cl2 | C. | C2H4O2 | D. |  |
5.警察常从案发现场的人体气味来获取有用线索.人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④乙酸乙酯;⑤十八烷;⑥己醛;⑦庚醛.下列说法正确的是( )
| A. | ①、②、⑥分子中碳原子数小于10,③、⑤分子中碳原子数大于10 | |
| B. | ①、②是无机物,③、⑤、⑦是有机物 | |
| C. | ①、④是酸,③、⑤不是酸 | |
| D. | ②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
12.有机物CH3-CH═CH-Cl能发生的反应是( )
①取代反应
②加成反应
③消去反应
④使溴水褪色
⑤使高锰酸钾酸性溶液褪色
⑥与AgNO3溶液生成白色沉淀
⑦加聚反应.
①取代反应
②加成反应
③消去反应
④使溴水褪色
⑤使高锰酸钾酸性溶液褪色
⑥与AgNO3溶液生成白色沉淀
⑦加聚反应.
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
9.下列说法不正确的是( )
| A. | 在熔融状态下,1molNa2O2完全电离出的离子数目为3NA(NA代表阿伏加德罗常数的值) | |
| B. | 酸性氧化物不一定是非金属氧化物,碱性氧化则一定是金属氧化物 | |
| C. | 常温下醋酸分子不可能存在于pH>7的碱性溶液中 | |
| D. | 第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
10.下列各组物质中,互为同位素的是( )
| A. | O2、O3 | B. | H2、D2、T2 | C. | H2O、D2O、T2O | D. | ${\;}_{1}^{1}$H ${\;}_{1}^{2}$H |
 ,该化合物是由离子键形成.
,该化合物是由离子键形成.