题目内容
根据下列框图分析.下列说法正确的是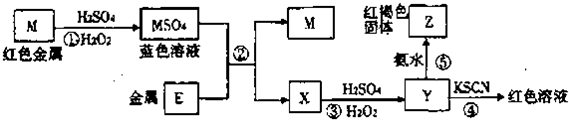
- A.E2+的氧化性比M2+的氧化性弱
- B.在反应①中硫酸既表现了酸性、又表现了氧化性
- C.反应④的离子方程式可表示为:3SCN-+E3+=E(SCN)3↓
- D.在③反应中若不加稀硫酸可能看到红褐色沉淀
AD
分析:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe;依据推断出的物质分析选项;
A、依据阳离子氧化性强弱,结合金属活动顺序表分析判断;Fe2+的氧化性比Cu2+的氧化性弱;
B、反应①中硫酸只是提供酸性环境,过氧化氢做氧化剂氧化铜;
C、反应④的离子方程式可表示为:3SCN-+Fe3+=Fe(SCN)3;生成的是血红色溶液,不是沉淀;
D、在③反应中若不加稀硫酸,硫酸亚铁被过氧化氢氧化为硫酸铁,在酸性溶液中铁离子会沉淀,可能看到红褐色沉淀;
解答:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe;
A、依据阳离子氧化性强弱,结合金属活动顺序表分析判断;Fe2+的氧化性比Cu2+的氧化性弱,故A正确;
B、反应①中硫酸只是提供酸性环境,过氧化氢做氧化剂氧化铜,故B错误;
C、反应④的离子方程式可表示为:3SCN-+Fe3+=Fe(SCN)3;生成的是血红色溶液,不是沉淀,故C错误;
D、在③反应中若不加稀硫酸,硫酸亚铁被过氧化氢氧化为硫酸铁,在酸性溶液中 铁离子会沉淀,可能看到红褐色沉淀,故D正确;
故选AD.
点评:本题考查了物质转化关系的推断和判断,物质性质的应用,反应现象的分析是解题关键,题目难度中等.
分析:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe;依据推断出的物质分析选项;
A、依据阳离子氧化性强弱,结合金属活动顺序表分析判断;Fe2+的氧化性比Cu2+的氧化性弱;
B、反应①中硫酸只是提供酸性环境,过氧化氢做氧化剂氧化铜;
C、反应④的离子方程式可表示为:3SCN-+Fe3+=Fe(SCN)3;生成的是血红色溶液,不是沉淀;
D、在③反应中若不加稀硫酸,硫酸亚铁被过氧化氢氧化为硫酸铁,在酸性溶液中铁离子会沉淀,可能看到红褐色沉淀;
解答:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe;
A、依据阳离子氧化性强弱,结合金属活动顺序表分析判断;Fe2+的氧化性比Cu2+的氧化性弱,故A正确;
B、反应①中硫酸只是提供酸性环境,过氧化氢做氧化剂氧化铜,故B错误;
C、反应④的离子方程式可表示为:3SCN-+Fe3+=Fe(SCN)3;生成的是血红色溶液,不是沉淀,故C错误;
D、在③反应中若不加稀硫酸,硫酸亚铁被过氧化氢氧化为硫酸铁,在酸性溶液中 铁离子会沉淀,可能看到红褐色沉淀,故D正确;
故选AD.
点评:本题考查了物质转化关系的推断和判断,物质性质的应用,反应现象的分析是解题关键,题目难度中等.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
 如图所示的A?G均为中学化学中常见的物质,它们之间有如下转化关系.其中A、G为非金属单质,且常温常压下A为黑色固体、G为气体;D、F都是大气污染物,主要来源于汽车尾气,而且D为红棕色.请冋答以下问题:
如图所示的A?G均为中学化学中常见的物质,它们之间有如下转化关系.其中A、G为非金属单质,且常温常压下A为黑色固体、G为气体;D、F都是大气污染物,主要来源于汽车尾气,而且D为红棕色.请冋答以下问题: Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)

 4AlCl3+3CO2↑
4AlCl3+3CO2↑