题目内容
19.下列实验“操作和现象”与“结论”对应关系正确的是( )| 操作和现象 | 结论 | |
| A | 常温下,将铝箔插入浓硝酸中,无明显现象 | 铝和浓硝酸不反应 |
| B | 用铂丝蘸取溶液进行焰色反应,观察到火焰呈黄色 | 该溶液一定是钠盐溶液 |
| C | 向酸性KMnO4溶液中通入SO2气体.酸性KMnO4溶液褪色 | SO2具有还原性 |
| D | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、Al箔表面被HNO3氧化,形成致密的氧化膜;
B、只能说明含有钠元素;
C、SO2具有还原性,能被强氧化剂氧化;
D、NO3-在酸性条件下具有氧化性,被还原生成NO,NO被O2氧化为红棕色的NO2.
解答 解:A、Al箔表面被HNO3氧化,形成致密的氧化膜,并不是没有反应,故A错误;
B、只能说明含有钠元素,不一定为钠盐,可能为碱溶液,故B错误;
C、SO2具有还原性,能被强氧化剂氧化,所以二氧化硫具有还原性,故C正确;
D、向Fe(NO3)2溶液中加入H2SO4,则会发生离子反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,产生的NO在管口生成NO2呈现红色,而不是HNO3分解产生NO2,故D错误;
故选C.
点评 本题考查化学实验方案的评价,涉及氧化还原反应、物质的检验等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型和高频考点,注意把握物质的性质的异同以及实验的合理性和可行性的评价,难度不大.

练习册系列答案
相关题目
9.将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)═2Z(g)△H<0.当改变某个条件并达到新平衡后,下列叙述正确的是( )
| A. | 升高温度,X的物质的量减小 | |
| B. | 增大压强(缩小容器体积),Z的浓度不变 | |
| C. | 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变 | |
| D. | 保持容器体积不变,充入一定量的Z,重新平衡时,Y的体积分数增大 |
10.下列有关化学用语表示正确的是( )
| A. | CF4的电子式: | B. | 对甲基苯酚的结构简式: | ||
| C. | 甲酸甲酯的实验式:CH2O | D. | ${\;}_{8}^{16}$O2-离子的结构示意图: |
7.下列有关化学用语表示正确的是( )
| A. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 氟原子的结构示意图: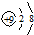 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同素异形体 | |
| D. | 碳酸钠的电离方程式:Na2CO3═Na2++CO32- |
14.下列无色透明水溶液中,能大量共存的一组离子是( )
| A. | K+、Mg2+、CO32-、Cl- | B. | Na+、Ba2+、HCO3-、OH- | ||
| C. | Mg2+、H+、Cl-、SO42- | D. | K+、SO42-、Cu2+、NO3- |
4.在实验室,下列试剂中需要用棕色试剂瓶保存的是( )
| A. | 浓硝酸 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 浓氨水 |
11.下列离子方程式书写正确的是( )
| A. | 稀硫酸与氢氧化钡溶液的反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 氢氧化铝与稀硝酸反应:Al(OH)3+3H+═Al3++3H2O | |
| D. | 钠与水反应:2Na+2H2O═2Na++OH-+H2↑ |
8.短周期元素W、X、Y、Z的原子序数依次增大,W的一种核素在考古时常用来鉴定一些文物的年代,X原子核外M电子层的电子数为1,Y是地壳中含量最高的金属元素,Z的单质可用于自来水的杀菌消毒.根据以上叙述,下列说法中正确的是( )
| A. | 四种元素的原子半径大小为W<X<Y<Z | |
| B. | 元素W与氢形成的原子比为1:1的化合物只有2种 | |
| C. | X、Y、Z的最高价氧化对应的水化物能相互反应 | |
| D. | 由W和Z组成的物质在熔融时能导电 |
17.有机化学中的反应类型较多,下列属于同一反应类型的是( )
| A. | 甲烷与氯气在光照的条件下反应,乙烯制氯乙烷 | |
| B. | 乙烷在氧气中燃烧,甲苯使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯水化法制乙醇,乙醇浓硫酸170℃制乙烯 | |
| D. | 乙块制氯乙烯,苯的溴代反应 |