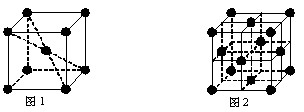题目内容
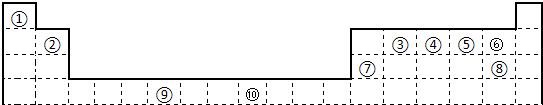
下图为长式周期表的一部分,其中的编号代表对应的元素.

请回答下列问题:
(1)表中属于ds区的元素是
(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是
(3)元素⑧的外围电子排布式为
(4)在周期表中位于对角线的元素的性质也有一定的相似性.试写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
(5)在1183K以下,元素⑨形成如图1所示基本结构单元的晶体;1183K以上,转变为图2所示基本结构单元的晶体.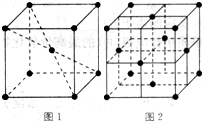
在1183K以下的晶体中,与元素⑨的原子等距离且最近的原子数为
在1183K以上的晶体中,与元素⑨的原子等距离且最近的原子数为

请回答下列问题:
(1)表中属于ds区的元素是
⑩
⑩
(填编号).(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是
sp
sp
;③和⑦形成的常见化合物的化学键类型是极性共价键
极性共价键
.(3)元素⑧的外围电子排布式为
3d54s1
3d54s1
,该元素原子中未成对电子数为6
6
.(4)在周期表中位于对角线的元素的性质也有一定的相似性.试写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
2NaOH+Be(OH)2═Na2BeO2+2H2O
2NaOH+Be(OH)2═Na2BeO2+2H2O
.(5)在1183K以下,元素⑨形成如图1所示基本结构单元的晶体;1183K以上,转变为图2所示基本结构单元的晶体.

在1183K以下的晶体中,与元素⑨的原子等距离且最近的原子数为
8
8
;在1183K以上的晶体中,与元素⑨的原子等距离且最近的原子数为
12
12
.分析:(1)元素周期表中位于ds区的元素为第ⅠB、ⅡB族,故符合的为⑩元素铜;
(2)元素①为氢元素,元素③为碳元素,元素⑦氯元素,根据题意可知,2个氢原子与的2个碳原子形成的分子中为乙烯,杂化类型是sp杂化,碳元素和氯元素形成化合物为四氯化碳,化学键类型是极性共价键;
(3)⑧为铬元素,价电子排布为3d54s1,六个电子均为单电子,故单电子数为 6个;
(4)根据对角线法则,铍元素与铝元素性质相似,氢氧化铍也为两性氢氧化物,可以与氢氧化钠反应生成相应的偏铍酸盐,化学方程式为2NaOH+Be(OH)2═Na2BeO2+2H2O;
(5)计算晶胞中原子个数,晶体中晶胞重复出现,推算到晶体中的原子个数.
(2)元素①为氢元素,元素③为碳元素,元素⑦氯元素,根据题意可知,2个氢原子与的2个碳原子形成的分子中为乙烯,杂化类型是sp杂化,碳元素和氯元素形成化合物为四氯化碳,化学键类型是极性共价键;
(3)⑧为铬元素,价电子排布为3d54s1,六个电子均为单电子,故单电子数为 6个;
(4)根据对角线法则,铍元素与铝元素性质相似,氢氧化铍也为两性氢氧化物,可以与氢氧化钠反应生成相应的偏铍酸盐,化学方程式为2NaOH+Be(OH)2═Na2BeO2+2H2O;
(5)计算晶胞中原子个数,晶体中晶胞重复出现,推算到晶体中的原子个数.
解答:解:(1)处于ds区的元素为第ⅠB和ⅡB,其中⑩位于第ⅠB,故属于ds区的元素为⑩,故答案为:⑩;
(2)元素①为氢元素,元素③为碳元素,2个氢原子与的2个碳原子形成的分子中为乙烯,元素碳的杂化类型是sp杂化;
元素③为碳元素和元素⑦氯元素形成的常见化合物为四氯化碳,四氯化碳的化学键类型是极性共价键,故答案为:sp;极性共价键;
(3)元素⑧为铬元素,位于第四周期第ⅥB族,价电子为六个,排布在s和d上,d上排五个电子形成半充满结构,比较稳定,故其外围电子排布式为3d54s1,六个电子均为单电子,故单电子数为 6个,故答案为:3d54s1;6;
(4)在周期表中位于对角线的元素的性质有一定的相似性,根据对角线法则,铍元素与铝元素具有一定的相似性,氢氧化铝为两性氢氧化物,故氢氧化铍也为两性氢氧化物,生成相应的偏铍酸盐,化学方程式为2NaOH+Be(OH)2═Na2BeO2+2H2O,故答案为:2NaOH+Be(OH)2═Na2BeO2+2H2O;
(5)在1183K以下,为左图所示,可知体心中有一个原子周围有八个原子,故每个晶胞中有8个原子与中心原子等距离且最近,在晶体中依然为8个,在1183K以上时为右图所示,以最上面中间原子为为例,同一个平面上有4个原子距离相等且距离最小,在竖直方向的四个面上,中间原子与所选定原子等距离且距离最小,在晶体中晶胞重复出现,故对面会有对称的四个竖直面上的点,一共12个,故答案为:8;12.
(2)元素①为氢元素,元素③为碳元素,2个氢原子与的2个碳原子形成的分子中为乙烯,元素碳的杂化类型是sp杂化;
元素③为碳元素和元素⑦氯元素形成的常见化合物为四氯化碳,四氯化碳的化学键类型是极性共价键,故答案为:sp;极性共价键;
(3)元素⑧为铬元素,位于第四周期第ⅥB族,价电子为六个,排布在s和d上,d上排五个电子形成半充满结构,比较稳定,故其外围电子排布式为3d54s1,六个电子均为单电子,故单电子数为 6个,故答案为:3d54s1;6;
(4)在周期表中位于对角线的元素的性质有一定的相似性,根据对角线法则,铍元素与铝元素具有一定的相似性,氢氧化铝为两性氢氧化物,故氢氧化铍也为两性氢氧化物,生成相应的偏铍酸盐,化学方程式为2NaOH+Be(OH)2═Na2BeO2+2H2O,故答案为:2NaOH+Be(OH)2═Na2BeO2+2H2O;
(5)在1183K以下,为左图所示,可知体心中有一个原子周围有八个原子,故每个晶胞中有8个原子与中心原子等距离且最近,在晶体中依然为8个,在1183K以上时为右图所示,以最上面中间原子为为例,同一个平面上有4个原子距离相等且距离最小,在竖直方向的四个面上,中间原子与所选定原子等距离且距离最小,在晶体中晶胞重复出现,故对面会有对称的四个竖直面上的点,一共12个,故答案为:8;12.
点评:本题考查了元素周期表中元素的分区;元素周期表中元素的位置;根据价电子数判断单电子个数;元素周期表中的对角线法则;晶胞及晶体中原子个数的计算.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
(12分)下表为长式周期表的一部分,其中的编号代表对应的元素。试填空。
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | | | | | | | | | | | | ⑦ | | | | ⑧ | |
| | | | | | ⑨ | | | ⑩ | | | | | | | | | |
(1)写出上表中元素⑨原子的外围电子排布式 。
(2)元素③与⑧形成的化合物中元素③的杂化方式为: 杂化,其形成的化合物的晶体类型是:______________ _ _。
(3)元素④、⑤的第一电离能大小顺序是: > (用元素符号表示);元素④与元素①形成的X分子的空间构型为: 。请写出与N3—互为等电子体的分子或离子的化学式 , (各写一种)。
(4)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应的化学方程式 。
(6)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为: 。