题目内容
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
反应一:Ni(粗,s)+4CO(g) Ni(CO)4(g) ΔH < 0
Ni(CO)4(g) ΔH < 0
反应二:Ni(CO)4(g) Ni(纯,s)+4CO(g) ΔH > 0
Ni(纯,s)+4CO(g) ΔH > 0
下列说法错误的是
| A.对于反应一,适当增大压强,有利于Ni(CO)4的生成 |
| B.提纯过程中,CO气体可循环使用 |
| C.升高温度,反应一的反应速率减小,反应二的速率增大 |
| D.对反应二,在180—200℃,温度越高,Ni(CO)4(g)的转化率越高 |
C
解析试题分析:A、增大压强,反应一平衡向右移动,正确;B、反应一CO作反应物。反应二生成了CO,所以CO气体可循环使用,正确;C、升高温度,所有化学反应的速率都增大,错误;D、反应二为吸热反应,温度升高,平衡向右移动,正确。
考点:本题考查条件对反应速率和化学平衡的影响、反应过程的分析。

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列说法正确的是 
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为: X(g)+Y(g) Z(g) Z(g) |
下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是
A.2NO2(g)  N2O4(g)△H<0 N2O4(g)△H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2 H I(g)△H<0 2 H I(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g)△H>0 NH3(g)+H2O(g)+CO2(g)△H>0 |
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g) ΔH<0,一段时间后达到平衡,反应过程中测定的数据如下表,下列说法正确的是
2Z(g) ΔH<0,一段时间后达到平衡,反应过程中测定的数据如下表,下列说法正确的是
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10—3mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)<v(正)
C.该温度下此反应的平衡常数K=144
D.其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
反应3X(g)+Y(g)  2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
| A.v(X)=0.05mol·L–1·min–1 | B.v(Z)=0.10mol·L–1·min–1 |
| C.v(Y)=0.10mol·L–1·min–1 | D.v(W)=0.05mol·L–1·min–1 |
在密闭容器中通入物质的量浓度均0.1mol·L-1的CH4与CO2,在一定条件下发生反应: ,测得CH4的平衡转化率与温度及压强的关系如图,下列有关说法一定正确的是
,测得CH4的平衡转化率与温度及压强的关系如图,下列有关说法一定正确的是
| A.上述反应的△H>0 |
| B.压强P1>P2>P3>P4 |
| C.1100℃该反应的平衡常数为64mol2·L-1 |
| D.压强为P4时,在Y点:v(正)<v(逆) |
已知 (CH3COOH)2 (g)  2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量(
2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量(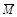 =
= )随温度(T)的变化曲线如图所示,下列说法正确的是
)随温度(T)的变化曲线如图所示,下列说法正确的是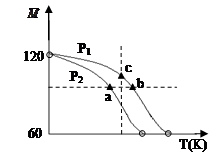
| A.该过程的△H < 0 |
| B.气体压强:P(a) < P(b) = P(c) |
| C.平衡常数:K(a) =" K(b)" < K(c) |
| D.测定乙酸的相对分子质量要在高压、低温条件 |


 ,5min内氨的质量增加了1.7g,则反应速率为( )
,5min内氨的质量增加了1.7g,则反应速率为( )



 C(g)+D(g)已达平衡状态的是( )
C(g)+D(g)已达平衡状态的是( )