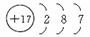题目内容
(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
|
Z |
|
|
Y |
X |
请回答:(1)三种元素中原子半径最大的是 (填X、Y或Z)
(2)若X的单质是黄绿色气体,则X和Y的最高价氧化物对应的水化物的酸性强弱顺序为 (用化学式表示),和X同主族元素氢化物中熔沸点最高的是 (用化学式表示),原因是 ;X单质溶于水生成物之一具有漂白性,写出该物质结构式 。
(3)若X的单质与强酸、强碱溶液反应均能放出氢气,则元素X在周期表中的位置 写出X单质和烧碱溶液反应的离子方程式
探究X和Y两种元素金属性强弱的实验方法是 。
(4)若Y的氧化物是制造光导纤维的材料,则Y元素的名称是 ,
工业上利用单质Z和Y的氧化物高温下反应,生成一种具有空间立体网状结构的化合物,另一种生成物是有毒气体,写出反应化学方程式 。
(1) Y 2分
(2)(每空格各 2分) H2SO4 < HClO4 HF
HF分子间形成氢键 H-O-Cl
(3)第三周期IIIA族 2分 2Al + 2OH-+2H2O = 2AlO2 - + 3H2↑ 2分
取形状大小相同的镁片和铝片分别与体积相同、浓度相同的稀盐酸反应,观察产生气泡的快慢 (3分)(操作2分,观察指标1分。着重号部分缺一处扣1分。用金属与沸水反应、等浓度盐溶液碱性比较等合理方法均得分)
(4)硅 2分 3C + SiO2 = 2CO ↑ + SiC 3分
【解析】

(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
| Z |
|
| Y | X |
请回答:(1)三种元素中原子半径最大的是 (填X、Y或Z)
(2)若X的单质是黄绿色气体,则X和Y的最高价氧化物对应的水化物的酸性强弱顺序为 (用化学式表示),和X同主族元素氢化物中熔沸点最高的是 (用化学式表示),原因是 ;X单质溶于水生成物之一具有漂白性,写出该物质结构式 。
(3)若X的单质与强酸、强碱溶液反应均能放出氢气,则元素X在周期表中的位置 写出X单质和烧碱溶液反应的离子方程式
探究X和Y两种元素金属性强弱的实验方法是 。
(4)若Y的氧化物是制造光导纤维的材料,则Y元素的名称是 ,
工业上利用单质Z和Y的氧化物高温下反应,生成一种具有空间立体网状结构的化合物,另一种生成物是有毒气体,写出反应化学方程式 。
(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
| Z | |
| Y | X |
(2)若X的单质是黄绿色气体,则X和Y的最高价氧化物对应的水化物的酸性强弱顺序为 (用化学式表示),和X同主族元素氢化物中熔沸点最高的是 (用化学式表示),原因是 ;X单质溶于水生成物之一具有漂白性,写出该物质结构式 。
(3)若X的单质与强酸、强碱溶液反应均能放出氢气,则元素X在周期表中的位置 写出X单质和烧碱溶液反应的离子方程式
探究X和Y两种元素金属性强弱的实验方法是 。
(4)若Y的氧化物是制造光导纤维的材料,则Y元素的名称是 ,
工业上利用单质Z和Y的氧化物高温下反应,生成一种具有空间立体网状结构的化合物,另一种生成物是有毒气体,写出反应化学方程式 。