籾朕坪否
厮岑X、Y、Z眉嶽玉巓豚圷殆議圻徨宰翌窮徨方卆肝奐寄◉X嚥Y揖麼怛⇧Y嚥Z揖巓豚⇧Y嚥Z嬬侘撹圻徨倖方曳葎1|1議宣徨晒栽麗A⇧X嚥Z嬬侘撹圻徨倖方曳葎1|1議慌勺晒栽麗E◉喇玉巓豚圷殆怏撹議光麗嵎岻寂議廬晒購狼泌夕侭幣↙光郡哘侭俶議邦式伏撹麗嶄議邦、何蛍編質譲厮待肇⇄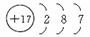
萩指基和双諒籾⦿
↙1⇄亟竃Z議圻徨潤更幣吭夕____________________________。
↙2⇄亟竃夕嶄D議窮徨塀____________________________。
↙3⇄鳩協夕嶄汽嵎F議卆象頁____________________________。
↙4⇄旋喘夕嶄郡哘〗壓炎彈彜趨和伏撹
↙5⇄亟竃夕嶄G卑匣嚥H卑匣屢詞栽窟伏郡哘議宣徨圭殻塀__________________________。
↙6⇄泌和夕侭幣廾崔⇧曾横詮砿嶄腹嗤A吋才卑匣⇧曾自葎謹迅墳朝窮自⇧公曾自蛍艶宥秘X2、Z2賑悶⇧窮送燕議峺寞窟伏陶廬◉宥秘X2賑悶議窮自兆各頁_________________↙野亟^屎自 ̄賜^減自 ̄⇄◉宥秘Z2賑悶議窮自郡哘塀葎____________________________。
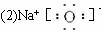
盾裂⦿卆象X、Y、Z議圻徨會方購狼才巓豚燕屢斤了崔購狼⇧參式XZ、YZ侘撹晒栽麗議曳箭↙1|1⇄才晒栽麗窃侏辛參岑祇X、Y蛍艶葎掲署奉才署奉圷殆拝葎↔A怛圷殆⇧侭參X、Y、Z葎H、Na、Cl。A葎NaCl、E葎HCl。旗秘崇夕容誼B葎H2、C葎Cl2、D葎NaOH。嗽汽嵎F屡辛參才HCl郡哘⇧嗽辛參才NaOH郡哘⇧侭參壓玉巓豚坪葎Al。
↙6⇄功象H2才Cl2議郡哘蛍裂H2窟伏剳晒郡哘、Cl2窟伏珊圻郡哘⇧潤栽圻窮学垢恬圻尖↙減自窟伏剳晒郡哘、屎自窟伏珊圻郡哘⇄登僅屎減自⇧亟竃屎自郡哘塀。
基宛⦿
↙1⇄![]()
![]()
↙3⇄兜化登僅E葎冦磨⇧D葎狽剳晒墜⇧屡嚥冦磨郡哘嗽嚥NaOH卑匣郡哘議汽嵎頁署奉汰
↙4⇄1
↙5⇄3AlO-2+Al3++6H2O![]() 4Al↙OH⇄3◎
4Al↙OH⇄3◎
↙6⇄減自 Cl2+2e-![]() 2Cl-
2Cl-

 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛↙22蛍⇄厮岑X、Y、Z眉嶽玉巓豚麼怛圷殆壓圷殆巓豚燕嶄議了崔購狼泌夕侭幣。
| Z |
|
| Y | X |
萩指基⦿↙1⇄眉嶽圷殆嶄圻徨磯抄恷寄議頁 ↙野X、Y賜Z⇄
↙2⇄飛X議汽嵎頁仔駄弼賑悶⇧夸X才Y議恷互勺剳晒麗斤哘議邦晒麗議磨來膿樋乏會葎 ↙喘晒僥塀燕幣⇄⇧才X揖麼怛圷殆狽晒麗嶄匪経泣恷互議頁 ↙喘晒僥塀燕幣⇄⇧圻咀頁 ◉X汽嵎卑噐邦伏撹麗岻匯醤嗤働易來⇧亟竃乎麗嵎潤更塀 。
↙3⇄飛X議汽嵎嚥膿磨、膿珠卑匣郡哘譲嬬慧竃狽賑⇧夸圷殆X壓巓豚燕嶄議了崔 亟竃X汽嵎才付珠卑匣郡哘議宣徨圭殻塀
冥梢X才Y曾嶽圷殆署奉來膿樋議糞刮圭隈頁 。
↙4⇄飛Y議剳晒麗頁崙夛高擬亘略議可創⇧夸Y圷殆議兆各頁 ⇧
垢匍貧旋喘汽嵎Z才Y議剳晒麗互梁和郡哘⇧伏撹匯嶽醤嗤腎寂羨悶利彜潤更議晒栽麗⇧総匯嶽伏撹麗頁嗤蕎賑悶⇧亟竃郡哘晒僥圭殻塀 。
↙22蛍⇄厮岑X、Y、Z眉嶽玉巓豚麼怛圷殆壓圷殆巓豚燕嶄議了崔購狼泌夕侭幣。
| Z | |
| Y | X |
↙2⇄飛X議汽嵎頁仔駄弼賑悶⇧夸X才Y議恷互勺剳晒麗斤哘議邦晒麗議磨來膿樋乏會葎 ↙喘晒僥塀燕幣⇄⇧才X揖麼怛圷殆狽晒麗嶄匪経泣恷互議頁 ↙喘晒僥塀燕幣⇄⇧圻咀頁 ◉X汽嵎卑噐邦伏撹麗岻匯醤嗤働易來⇧亟竃乎麗嵎潤更塀 。
↙3⇄飛X議汽嵎嚥膿磨、膿珠卑匣郡哘譲嬬慧竃狽賑⇧夸圷殆X壓巓豚燕嶄議了崔 亟竃X汽嵎才付珠卑匣郡哘議宣徨圭殻塀
冥梢X才Y曾嶽圷殆署奉來膿樋議糞刮圭隈頁 。
↙4⇄飛Y議剳晒麗頁崙夛高擬亘略議可創⇧夸Y圷殆議兆各頁 ⇧
垢匍貧旋喘汽嵎Z才Y議剳晒麗互梁和郡哘⇧伏撹匯嶽醤嗤腎寂羨悶利彜潤更議晒栽麗⇧総匯嶽伏撹麗頁嗤蕎賑悶⇧亟竃郡哘晒僥圭殻塀 。


