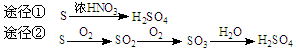题目内容
稀硫酸中加入铜片,无现象,再加入下列某物质后,铜片逐渐溶解,该物质为
| A.KNO3 | B.NaCl | C.FeCl3 | D.Cu(OH)2 |
AC
分析:根据铜的化学性质,铜不能与弱氧化性酸反应,但可以和强氧化性酸反应,能与具有氧化性的FeCl3溶液、酸性条件下硝酸盐等反应,据此判断选项.
解答:解:A、铜与稀HNO3反应,该反应的离子方程式:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,可知Cu遇到H+、NO3-能发生氧化还原反应,向稀硫酸溶液中加入硝酸钾后,溶液中存在氢离子和硝酸根离子,所以铜能溶解,故A正确;
B、向稀硫酸溶液中加入氯化钠后,溶液中不存在与铜反应的物质,故B错误.
C、向稀硫酸溶液中加入氯化铁后,氯化铁有氧化性,能把铜氧化成铜离子,所以铜能溶解,故C正确.
D、向稀硫酸溶液中加入氢氧化铜后,氢氧化铜是碱能和酸反应生成盐和水,但氢氧化铜和铜不反应,所以铜不溶解,故D错误.
故选AC.
解答:解:A、铜与稀HNO3反应,该反应的离子方程式:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,可知Cu遇到H+、NO3-能发生氧化还原反应,向稀硫酸溶液中加入硝酸钾后,溶液中存在氢离子和硝酸根离子,所以铜能溶解,故A正确;
B、向稀硫酸溶液中加入氯化钠后,溶液中不存在与铜反应的物质,故B错误.
C、向稀硫酸溶液中加入氯化铁后,氯化铁有氧化性,能把铜氧化成铜离子,所以铜能溶解,故C正确.
D、向稀硫酸溶液中加入氢氧化铜后,氢氧化铜是碱能和酸反应生成盐和水,但氢氧化铜和铜不反应,所以铜不溶解,故D错误.
故选AC.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目