题目内容
 某兴趣小组采用如下方法制作氢氧燃料电池.
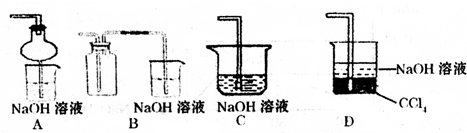
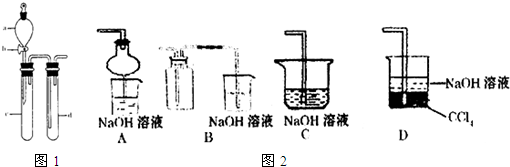
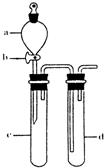
某兴趣小组采用如下方法制作氢氧燃料电池.(1)如图A所示:a、b均为多孔石墨棒(多孔石墨棒,可吸附并储存生成的气体),其中a与直流电源正极相连,b与直流电源负极相连,电解质溶液为NaOH溶液,则a电极上发生的电极反应式为
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
,电解后溶液的pH增大
增大
(填“增大”、“减小”或“不变”).(2)然后如图B所示,移走直流电源,在a、b极间连接一个发光二极管,可以看到二极管发光.此时的电流方向是
a→b
a→b
(填“a→b”或“b→a”),b极的电极反应式为H2+2OH--2e-=2H2O
H2+2OH--2e-=2H2O
.(3)假设a极吸收22.4L(标准状况)气体,能量转化率为60%,则通过二极管的电子的物质的量为
2.4mol
2.4mol
.分析:(1)A装置图是电解池装置,依据电源的正负极分析判断电极,a为阳极;b为阴极;结合电解质溶液是强碱溶液,惰性电极电极氢氧化钠溶液实质电解水,氢氧化钠溶液浓度增大,依据离子放电写出电极反应;
(2)图B是原电池装置,依据电解过程生成气体可知,a电极生成的是氧气;b电极生成的是氢气,去掉电源连接发光二极管,可以看到二极管发光,说明氢气和氧气再氢氧化钠溶液中形成了燃料电池,氧气一端做正极,氢气一端做负极;电流方向从正极流向负极;
(3)依据原电池中电极反应的电子守恒计算得到.
(2)图B是原电池装置,依据电解过程生成气体可知,a电极生成的是氧气;b电极生成的是氢气,去掉电源连接发光二极管,可以看到二极管发光,说明氢气和氧气再氢氧化钠溶液中形成了燃料电池,氧气一端做正极,氢气一端做负极;电流方向从正极流向负极;
(3)依据原电池中电极反应的电子守恒计算得到.
解答:解:(1)A装置图是电解池装置,依据电源的正负极分析判断电极,a为阳极;b为阴极;结合电解质溶液是强碱溶液,惰性电极电极氢氧化钠溶液实质电解水,氢氧化钠溶液浓度增大,溶液PH增大,a电极为阳极,电极反应为:4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;增大;
(2)图B是原电池装置,依据电解过程生成气体可知,a电极生成的是氧气;b电极生成的是氢气,去掉电源连接发光二极管,可以看到二极管发光,说明氢气和氧气再氢氧化钠溶液中形成了燃料电池,氧气一端做正极,氢气一端做负极;电流方向从正极流向负极,即a→b;b极为原电池负极,氢气是电子发生氧化反应,电解质溶液是氢氧化钠溶液,电极反应式为:H2+2OH--2e-=2H2O,故答案为:a→b;H2+2OH--2e-=2H2O;
(3)a极吸收22.4L(标准状况)气体物质的量为1mol,b电极为负极,电极反应:H2+2OH--2e-=2H2O;a电极为正极,电极反应:O2+2H2O=4e-=4OH-;a电极吸收氧气1mol,电子转移为4mol,能量转化率为60%,所以实际转移的电子物质的量为4mol×60%=2.4mol,故答案为:2.4mol.
(2)图B是原电池装置,依据电解过程生成气体可知,a电极生成的是氧气;b电极生成的是氢气,去掉电源连接发光二极管,可以看到二极管发光,说明氢气和氧气再氢氧化钠溶液中形成了燃料电池,氧气一端做正极,氢气一端做负极;电流方向从正极流向负极,即a→b;b极为原电池负极,氢气是电子发生氧化反应,电解质溶液是氢氧化钠溶液,电极反应式为:H2+2OH--2e-=2H2O,故答案为:a→b;H2+2OH--2e-=2H2O;
(3)a极吸收22.4L(标准状况)气体物质的量为1mol,b电极为负极,电极反应:H2+2OH--2e-=2H2O;a电极为正极,电极反应:O2+2H2O=4e-=4OH-;a电极吸收氧气1mol,电子转移为4mol,能量转化率为60%,所以实际转移的电子物质的量为4mol×60%=2.4mol,故答案为:2.4mol.
点评:本题考查了电解池、原电池的原理应用,电子守恒的计算应用,电极判断,电极名称,电极反应的分析判断是解题关键,题目较简单.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
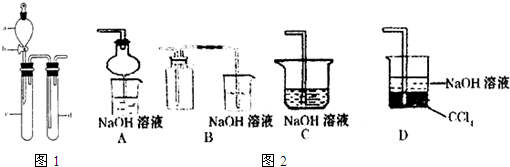
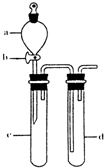 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.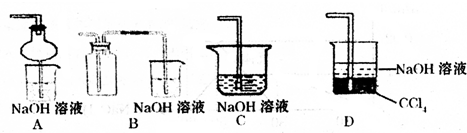

 生产流程,其流程示意图如下:
生产流程,其流程示意图如下:

 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.