题目内容
11.胡妥油(D)用作香料的原料,它可由A合成得到( )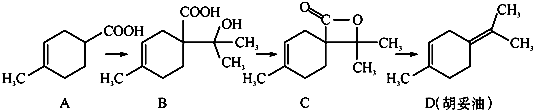
| A. | 从B到C的反应是消去反应 | |
| B. | D分子中所有碳原子一定共面 | |
| C. | 等物质的量的B分别与足量的Na、NaHCO3反应,产生的气体的物质的量前者大于后者 | |
| D. | 若A是由2-甲基-1,3-丁二烯和丙烯酸(CH2=CHCOOH)加热得到的,则该反应的类型属于加成反应 |
分析 A.从B到C的反应是酯化反应;
B.有机物D中环状结构含3个亚甲基,为四面体结构;
C.B含有羧基、羟基,都可与钠反应,只有羧基与碳酸氢钠反应;
D.异戊二烯和丙烯酸发生加成反应生成有机物A.
解答 解:A.B含有羟基、羧基,C含有酯基,从B到C的反应是酯化反应,故A错误;
B.有机物D中环状结构含3个亚甲基,为四面体结构,则所以碳原子不会共面,故B错误;
C.B含有羧基、羟基,都可与钠反应,只有羧基与碳酸氢钠反应,等物质的量的B分别与足量的Na、NaHCO3反应,产生的气体相等,故C错误;
D.异戊二烯和丙烯酸发生类似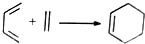 的加成反应生成有机物A,故D正确.
的加成反应生成有机物A,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、醇性质及同分异构体的考查,选项BD为易错点,题目难度不大.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
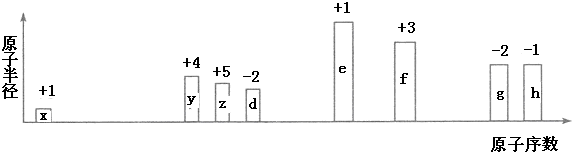
2.已知短周期元素的离子.aAm+、bBn+、cCm-、dDn-(m>n)都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 离子半径:C>D>B>A | ||
| C. | 原子序数:d>c>b>a | D. | 最外层电子数:D>C>B>A |
19.下列叙述能说明氯元素原子得电子能力比硫元素强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强
③HCl的稳定性比H2S强 ④还原性:Cl-<S2-
⑤HClO4的酸性比H2SO4强 ⑥单质熔点:S>Cl2
⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
⑨Cl2与铁反应生成FeCl3,而S与铁反应生成FeS.
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强
③HCl的稳定性比H2S强 ④还原性:Cl-<S2-
⑤HClO4的酸性比H2SO4强 ⑥单质熔点:S>Cl2
⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
⑨Cl2与铁反应生成FeCl3,而S与铁反应生成FeS.
| A. | ③④⑤⑦⑧⑨ | B. | ③⑤⑥⑦⑧⑨ | C. | ②③④⑤⑦⑧ | D. | ①②④⑥⑧⑨ |
6.下列各组化合物,不论二者以什么比例混合,只要总质量一定,则完全燃烧时,消耗O2的质量和生成水的质量不变的是( )
| A. | CH4 C2H2 | B. | C2H6 C3H6 | C. | C2H4 C3H6 | D. | C2H4 C3H4 |
20.在HI溶液中滴加淀粉溶液无明显变化,但加入某种物质后,溶液立即变蓝.该物质可能是( )
| A. | FeCl3 | B. | K2SO3 | C. | NaOH | D. | Na2S |
1.下列单质氧化性最强的是( )
| A. | F2 | B. | Cl2 | C. | Br2 | D. | I2 |
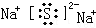 .化合物中离子半径较大的是S2-(填离子符号).
.化合物中离子半径较大的是S2-(填离子符号).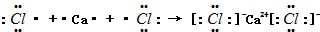 ;
;