题目内容
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8kJ/mol
CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0kJ/mol
C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(l)
ΔH=-5518 kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)
ΔH=-890.3kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是()。
A.H2(g) B.CO(g)
C.C8H18(l) D.CH4(g)
B
【试题分析】

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目

 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题: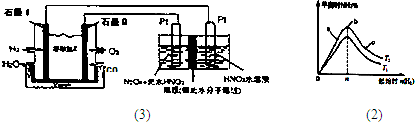
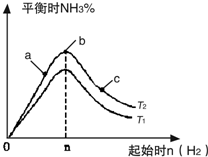 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题: