题目内容
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)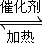 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
【答案】分析:(1)升高温度,可逆反应向吸热反应方向移动,根据平衡常数与温度变化关系确定焓变;
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,据此解答,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)①根据SO2的转化率计算参加反应的SO2的物质的量,利用物质的量之比等于化学计量数之比计算反应的O2的物质的量,再根据v=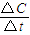 计算v(O2);
计算v(O2);
②根据二氧化硫的转化率来分析;
③计算平衡时各组分的平衡浓度,代入平衡常数表达式计算;
(4)压强增大,平衡向气体体积减少的方向移动.
解答:解:(1)升高温度,平衡向吸热方向移动,根据表格知,温度越高,化学平衡常数越小,说明平衡向逆反应方向移动,所以正反应是放热反应,即△H<0,
故答案为:<;
(2)A.随反应进行气体的物质的量减少,压强减少,容器中压强不变,说明到达平衡状态,故A正确;
B.随反应进行气体的质量不变,容器的体积也不变,密度不变,混合气体的密度不变,不能说明到达平衡状态,故B错误;
C.混合气体中SO3的浓度不变,能说明到达平衡状态,故C正确;
D.反应到达平衡时个物质的浓度不变,但不一定C(SO2)=C(SO3),所以不能作为达平衡状态的标志,故D错误;
E.在任何时刻v正(SO2)=v正(SO3),所以不能作为达平衡状态的标志,故E错误;
F.v正(SO3)=2v逆(O2)不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,故F正确;
故选:ACF;
(3)①参加反应的SO2的浓度0.4mol?L-1-0.08mol?L-1=0.32mol?L-1,故参加反应的O2为0.32mol?L-1× =0.16mol?L-1,故v(O2)=
=0.16mol?L-1,故v(O2)=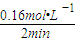 =0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;
=0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;
②二氧化硫的转化率为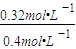 ×100%=80%,所以此时的温度为600℃,故答案为:600;
×100%=80%,所以此时的温度为600℃,故答案为:600;
③2SO2(g)+O2(g)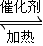 2SO3(g),
2SO3(g),
反应开始(mol/L) 0.4 1 0
反应(mol/L) 0.32 0.16 0.32
平衡 (mol/L) 0.08 0.84 0.32
平衡常数K=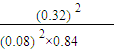 =
=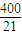 ,
,
故答案为: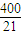 ;
;
(4)该反应正向是一个气体体积减少的反应,所以压强增大,平衡向正反应方向移动,故答案为:正.
点评:本题考查了影响化学平衡移动的因素、平衡状态的判断、反应速率的计算、平衡常数的计算等知识点,注意利用三段式计算平衡时各组分的平衡浓度,代入平衡常数表达式计算.
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,据此解答,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)①根据SO2的转化率计算参加反应的SO2的物质的量,利用物质的量之比等于化学计量数之比计算反应的O2的物质的量,再根据v=
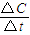 计算v(O2);
计算v(O2);②根据二氧化硫的转化率来分析;
③计算平衡时各组分的平衡浓度,代入平衡常数表达式计算;
(4)压强增大,平衡向气体体积减少的方向移动.
解答:解:(1)升高温度,平衡向吸热方向移动,根据表格知,温度越高,化学平衡常数越小,说明平衡向逆反应方向移动,所以正反应是放热反应,即△H<0,
故答案为:<;
(2)A.随反应进行气体的物质的量减少,压强减少,容器中压强不变,说明到达平衡状态,故A正确;
B.随反应进行气体的质量不变,容器的体积也不变,密度不变,混合气体的密度不变,不能说明到达平衡状态,故B错误;
C.混合气体中SO3的浓度不变,能说明到达平衡状态,故C正确;
D.反应到达平衡时个物质的浓度不变,但不一定C(SO2)=C(SO3),所以不能作为达平衡状态的标志,故D错误;
E.在任何时刻v正(SO2)=v正(SO3),所以不能作为达平衡状态的标志,故E错误;
F.v正(SO3)=2v逆(O2)不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,故F正确;
故选:ACF;
(3)①参加反应的SO2的浓度0.4mol?L-1-0.08mol?L-1=0.32mol?L-1,故参加反应的O2为0.32mol?L-1×
 =0.16mol?L-1,故v(O2)=
=0.16mol?L-1,故v(O2)=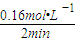 =0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;
=0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;②二氧化硫的转化率为
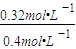 ×100%=80%,所以此时的温度为600℃,故答案为:600;
×100%=80%,所以此时的温度为600℃,故答案为:600;③2SO2(g)+O2(g)
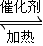 2SO3(g),
2SO3(g),反应开始(mol/L) 0.4 1 0
反应(mol/L) 0.32 0.16 0.32
平衡 (mol/L) 0.08 0.84 0.32
平衡常数K=
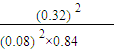 =
=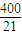 ,
,故答案为:
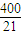 ;
;(4)该反应正向是一个气体体积减少的反应,所以压强增大,平衡向正反应方向移动,故答案为:正.
点评:本题考查了影响化学平衡移动的因素、平衡状态的判断、反应速率的计算、平衡常数的计算等知识点,注意利用三段式计算平衡时各组分的平衡浓度,代入平衡常数表达式计算.

练习册系列答案
相关题目