题目内容
某校学生小组进行硫酸铜品体里结晶水含量的测定实验,其实验步骤如下:①用坩埚准确称取2.0 g硫酸铜晶体,记下坩埚和硫酸铜晶体的总质馈m1;
②将盛有硫酸铜品体的坩埚放在三角架上而的泥三角上,缓慢加热,直到蓝色的硫酸铜品体完全变成白色,且不再有水蒸气逸出,然后将坩埚冷却;
③待坩埚冷却后,将坩埚放在天平上称量,记下坩埚和无水硫酸铜的总质量m2。
(1)②中加热硫酸铜晶体时所用的仪器有____________________________________________。
(2)上述每一步实验中,都有一个很关键的步骤没有给出,它们是①______________________;②_________________________;③____________________________。
(3)写出硫酸铜晶体(CuSO4·xH2O)中结晶水的表达式x=_______________________。
(4)该小组最终测定的结果偏高,其原因可能是(选填字母序号)________________________。
A.取出的硫酸铜晶体未研成粉末,就开始加热
B.在①中称量坩埚和硫酸铜晶体时,天平指针偏右
C.加热时,硫酸铜晶体刚变为白色,就停止加热
D.将加热后的白色粉末放在空气中冷却
(1)坩埚、泥三角、三角架、酒精灯、玻璃棒
(2)①将硫酸铜晶体研成粉末;②要放在干燥器中冷却;③多次加热至连续两次称量的质量差不超过0.
(3)![]()
(4)B

 全能练考卷系列答案
全能练考卷系列答案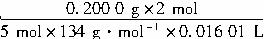
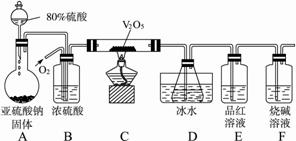
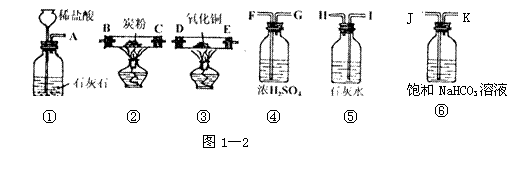
(1)装置C中盛放NaOH溶液的作用是__________________________________。
(2)①证明分解产物中有CO2的现象是__________________________________。
②证明分解产物中有CO的现象是_____________________________________。
(3)实验结束后,装置F中黑色氧化铜变为红色固体。简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):_____________________________________________________________________。
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4、MnO2氧化。KMnO4和草酸钠在稀硫酸中反应的离子方程式是______________________________________________。
②实验室常用草酸钠标定KMnO4溶液。操作如下:准确称取0.200 0 g草酸钠,放入锥形瓶中,加100 mL稀硫酸溶解,用配置好的KMnO4溶液滴定。当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30 s内不褪色,即达到滴定终点。重复上述滴定操作三次,实验数据如下表所示。
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 |
滴定管液面刻度 | 0.00 mL | 16.02 mL | 16.00 mL | 16.01 mL |
KMnO4溶液的物质的量浓度的计算式是:?
c(KMnO4)=_________________。