题目内容
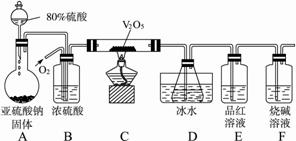
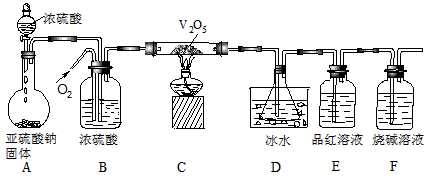
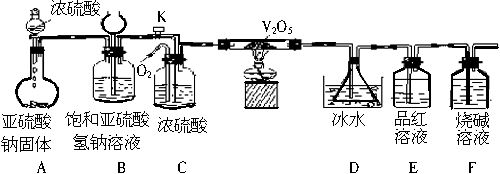
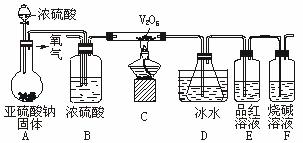
某校学生活动小组设计如图所示装置探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。
试填空:(1)装置B的三个作用是①__________;②__________;③__________。
(2)实验过程中,当V2O5表面红热后,应将酒精灯移开一会儿后再继续加热,其原因是__________。
(3)D中锥形瓶中盛放的溶液可以是(选填序号)__________。
①足量澄清石灰水 ②足量小苏打溶液 ③足量氯化钡溶液 ④足量硝酸钡溶液
反应停止后,再根据装置D锥形瓶中产生的白色沉淀的量,测定已被氧化的二氧化硫的量时,在滤出沉淀前必须进行的一步实验操作是(简述过程) ______________________________。
(4)若从锥形瓶溶液中得到的沉淀质量为m g,要测定该条件下二氧化硫的转化率,实验时还需要测定的数据是__________ (选填序号),二氧化硫的转化率是__________ (用含有m、a、b、c、d中的一种或几种字母的代数式表示)。
①装置F增加的质量a g ②装置A中亚硫酸钠减少的质量b g ③装置B增加的质量c g ④装置E增加的质量为d g
解析:D中生成的是![]() 的沉淀,Ba(NO3)2与SO2、SO3与水溶液作用生成HNO3,HNO3又把+4价的硫氧化了,因此不能测定SO2的转化率,因此D中装的物质应为BaCl2溶液。装置E、F中吸收SO2,则SO2的转化率易知。
的沉淀,Ba(NO3)2与SO2、SO3与水溶液作用生成HNO3,HNO3又把+4价的硫氧化了,因此不能测定SO2的转化率,因此D中装的物质应为BaCl2溶液。装置E、F中吸收SO2,则SO2的转化率易知。
答案:(1)①干燥氧气和二氧化硫 ②使氧气和二氧化硫混合均匀 ③便于通过观察气泡的速率,控制氧气和二氧化硫的比例
(2)该反应的正反应放热,温度过高平衡逆向移动,不利于三氧化硫的生成;且影响催化剂的活性
(3)③ 向锥形瓶中滴加氯化钡溶液,直至沉淀量不再增加(或“静置后向上层清液中滴入氯化钡溶液,若产生沉淀,继续加入氯化钡溶液,重复上述过程直至清液中不再产生沉淀”)
(4)①④ 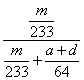 ×100%
×100%