题目内容
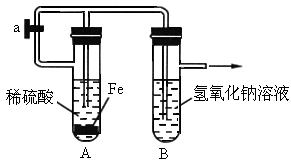
按下图所示装置,用两种不同操作分别进行实验,观察B管中的现象.

操作1:先夹紧止水夹a,再使A管开始反应,实验中在B管中观察到的现象是:_________,B管中发生反应的离子方程式是:________;
操作2:打开止水夹a,使A管开始反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是_________.B管中发生反应的离子方程式是:_____________.
答案:略
解析:
提示:
解析:
|
产生白色絮状沉淀,迅速变为灰绿色,最后变为红褐色沉淀; 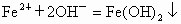 , ,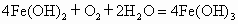 ;开始时B管口有气泡产生,夹紧止水夹a后产生白色絮状沉淀,一定时间内沉淀颜色没有变化; ;开始时B管口有气泡产生,夹紧止水夹a后产生白色絮状沉淀,一定时间内沉淀颜色没有变化;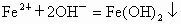 . . |
提示:
|
先夹紧止水夹 a,Fe与稀 反应产生的 反应产生的 使试管A中气压增大,将生成的溶液压入到试管B中, 使试管A中气压增大,将生成的溶液压入到试管B中, 跟NaOH反应生成 跟NaOH反应生成 ,并迅速被氧化成 ,并迅速被氧化成 ;若先反应一段时间,试管A中空气被排出, ;若先反应一段时间,试管A中空气被排出, 跟NaOH反应生成的白色絮状沉淀会保持一段时间. 跟NaOH反应生成的白色絮状沉淀会保持一段时间. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目