题目内容
为探究SO2与BaCl2溶液间能否反应,甲、乙两同学设计了如下实验方案.请你协助完成.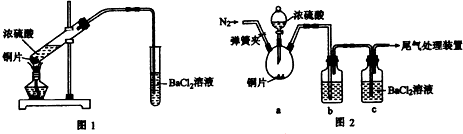
(1)甲同学设计了如图1所示装置,其中浓硫酸的沸点为338℃,酒精灯外焰温度为500℃,反应一段时间后发现BaCl2溶液中出现了不溶于盐酸的白色沉淀.
①加热时左试管中发生反应的化学方程式为 .
②白色沉淀的成分是 ,生成白色沉淀的原因可能是 (选填字母序号)
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
c.SO2溶于水生成的H2SO3被空气中的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀
(2)乙同学设计了如图2所示装置,其中夹持及加热装置已省略,装置的气密性良好.
①打开弹簧夹,通入N2一段时间后关闭弹簧夹.其目的是 .
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀.洗气瓶b中试剂是 ,其作用是 .
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,反应的离子方程式为 .
(3)你认为上述两个方案中比较合理的是 (选填“甲”或“乙”),理由是 .

(1)甲同学设计了如图1所示装置,其中浓硫酸的沸点为338℃,酒精灯外焰温度为500℃,反应一段时间后发现BaCl2溶液中出现了不溶于盐酸的白色沉淀.
①加热时左试管中发生反应的化学方程式为
②白色沉淀的成分是
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
c.SO2溶于水生成的H2SO3被空气中的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀
(2)乙同学设计了如图2所示装置,其中夹持及加热装置已省略,装置的气密性良好.
①打开弹簧夹,通入N2一段时间后关闭弹簧夹.其目的是
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀.洗气瓶b中试剂是
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,反应的离子方程式为
(3)你认为上述两个方案中比较合理的是
分析:(1)①左图装置中是铜和浓硫酸加热反应生成二氧化硫的发生装置;
②通入氯化钡溶液中生成溶于盐酸的白色沉淀为硫酸钡;结合选项分析可能的原因,温度过高,发生装置中挥发出硫酸蒸气,或二氧化硫和水反应生成亚硫酸钡氧化为硫酸形成硫酸钡白色沉淀;
(2)①装置中空气的存在会干扰实验需要排除,氮气是不活泼的气体,可以利用氮气排净装置中的空气;
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀,说明生成的二氧化硫气体中不含硫酸蒸气;需要用装置b中的饱和亚硫酸氢钠溶液吸收;
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,说明装置c中溶解的二氧化硫被过氧化氢氧化为硫酸,结合氯化钡反应生成白色沉淀硫酸钡;
(3)分析上述实验验证过程,乙装置排除了空气的影响,除去硫酸蒸气,避免对后续实验的干扰.
②通入氯化钡溶液中生成溶于盐酸的白色沉淀为硫酸钡;结合选项分析可能的原因,温度过高,发生装置中挥发出硫酸蒸气,或二氧化硫和水反应生成亚硫酸钡氧化为硫酸形成硫酸钡白色沉淀;
(2)①装置中空气的存在会干扰实验需要排除,氮气是不活泼的气体,可以利用氮气排净装置中的空气;
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀,说明生成的二氧化硫气体中不含硫酸蒸气;需要用装置b中的饱和亚硫酸氢钠溶液吸收;
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,说明装置c中溶解的二氧化硫被过氧化氢氧化为硫酸,结合氯化钡反应生成白色沉淀硫酸钡;
(3)分析上述实验验证过程,乙装置排除了空气的影响,除去硫酸蒸气,避免对后续实验的干扰.
解答:解:(1)①左图装置中是铜和浓硫酸加热反应生成二氧化硫的发生装置,反应的化学方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
②通入氯化钡溶液中生成不溶于盐酸的白色沉淀为硫酸钡;结合选项分析可能的原因,温度过高,发生装置中挥发出硫酸蒸气,或二氧化硫和水反应生成亚硫酸钡氧化为硫酸形成硫酸钡白色沉淀;
a.SO2与BaCl2溶液不反应,反应过程中不能生成白色沉淀,故a错误;
b.高温下挥发出硫酸蒸气,BaCl2溶液与硫酸蒸气反应生成了白色沉淀硫酸钡,故b正确;
c.SO2溶于水生成的H2SO3被空气中的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀,符合实验现象,故c正确;
故答案为:bc;
(2)①装置中空气的存在会干扰实验需要排除,氮气是不活泼的气体,可以利用氮气排净装置中的空气,
故答案为:排除装置内的空气;
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀,说明生成的二氧化硫气体中不含硫酸蒸气;需要用装置b中的饱和亚硫酸氢钠溶液吸收,
故答案为:饱和亚硫酸氢钠溶液,除去挥发出的硫酸蒸气;
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,说明装置c中溶解的二氧化硫被过氧化氢氧化为硫酸,结合氯化钡反应生成白色沉淀硫酸钡,反应的离子方程式为:Ba2++SO2+H2O2=BaSO4↓+2H+;
故答案为:Ba2++SO2+H2O2=BaSO4↓+2H+;
(3)分析上述实验验证过程,乙装置排除了空气的影响,除去硫酸蒸气,避免对后续实验的干扰,所以乙方案更合理,乙方案中除去了可能产生干扰的硫酸蒸气和空气,使实验结果更为准确,
故答案为:乙,乙方案中除去了可能产生干扰的硫酸蒸气和空气,使实验结果更为准确.
| ||
故答案为:Cu+2H2SO4(浓)
| ||
②通入氯化钡溶液中生成不溶于盐酸的白色沉淀为硫酸钡;结合选项分析可能的原因,温度过高,发生装置中挥发出硫酸蒸气,或二氧化硫和水反应生成亚硫酸钡氧化为硫酸形成硫酸钡白色沉淀;
a.SO2与BaCl2溶液不反应,反应过程中不能生成白色沉淀,故a错误;
b.高温下挥发出硫酸蒸气,BaCl2溶液与硫酸蒸气反应生成了白色沉淀硫酸钡,故b正确;
c.SO2溶于水生成的H2SO3被空气中的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀,符合实验现象,故c正确;
故答案为:bc;
(2)①装置中空气的存在会干扰实验需要排除,氮气是不活泼的气体,可以利用氮气排净装置中的空气,
故答案为:排除装置内的空气;
②滴加一定量浓硫酸,加热a,一段时间后c中没有出现白色沉淀,说明生成的二氧化硫气体中不含硫酸蒸气;需要用装置b中的饱和亚硫酸氢钠溶液吸收,
故答案为:饱和亚硫酸氢钠溶液,除去挥发出的硫酸蒸气;
③取实验后c中溶液少许,逐滴加入H2O2溶液,生成了不溶于盐酸的白色沉淀,说明装置c中溶解的二氧化硫被过氧化氢氧化为硫酸,结合氯化钡反应生成白色沉淀硫酸钡,反应的离子方程式为:Ba2++SO2+H2O2=BaSO4↓+2H+;
故答案为:Ba2++SO2+H2O2=BaSO4↓+2H+;
(3)分析上述实验验证过程,乙装置排除了空气的影响,除去硫酸蒸气,避免对后续实验的干扰,所以乙方案更合理,乙方案中除去了可能产生干扰的硫酸蒸气和空气,使实验结果更为准确,
故答案为:乙,乙方案中除去了可能产生干扰的硫酸蒸气和空气,使实验结果更为准确.
点评:本题考查了物质性质的实验验证分析判断,物质性质的分析,装置特征的判断,反应条件的应用是解题关键,题目难度中等.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目

 ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。