题目内容
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、1mol甲苯含有6NA个C-H键 |
| B、18gH2O含有10NA个质子 |
| C、标准状况下,22.4L乙醇的分子数为NA |
| D、电解精炼铜过程中,电路中每通过NA个电子,阳极溶解铜32g |
考点:阿伏加德罗常数
专题:
分析:A.苯分子中的碳碳键是介于单键与双键之间独特的化学键;
B.1个水分子含有10个质子;
C.气体摩尔体积适用对象为气体;
D.粗铜精炼时,阳极为粗铜,比铜活泼的金属锌、铁等先失去电子;
B.1个水分子含有10个质子;
C.气体摩尔体积适用对象为气体;
D.粗铜精炼时,阳极为粗铜,比铜活泼的金属锌、铁等先失去电子;
解答:
解:A.苯分子不含碳碳单键,故A错误;
B.18gH2O的物质的量为1mol,含有10NA个质子,故B正确;
C.标况下乙醇为液体,不能使用气体摩尔体积,故C错误;
D.由Cu-2e=Cu2+,32g铜的物质的量为0.5mol,则转移电子数为6.02×1023个,但在阳极比铜活泼的金属锌、铁等先失去电子,则转移电子数大于6.02×1023个,故D错误;
故选:B.
B.18gH2O的物质的量为1mol,含有10NA个质子,故B正确;
C.标况下乙醇为液体,不能使用气体摩尔体积,故C错误;
D.由Cu-2e=Cu2+,32g铜的物质的量为0.5mol,则转移电子数为6.02×1023个,但在阳极比铜活泼的金属锌、铁等先失去电子,则转移电子数大于6.02×1023个,故D错误;
故选:B.
点评:本题考查阿伏加德罗常数的应用,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态即可解答,题目难度不大.

练习册系列答案
相关题目
某有机物的结构简式如图所示,1mol该有机物与足量的NaOH溶液共热,充分反应后最多可消耗NaOH的物质的量为( )


| A、2mol | B、4mol |
| C、6mol | D、8mol |
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一.下列有关元素周期表的说法正确的是( )
| A、元素周期表有7个周期 |
| B、元素周期表有18个族 |
| C、第ⅠA族的元素全部是金属元素 |
| D、短周期是指第1、2、3、4周期 |
下列化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 | ||
B、S2-的结构示意图: | ||
C、中子数为20的氯原子:
| ||
D、羟基的电子式: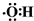 |
下列物质中不属于 有机物的是( )
| A、CH4 |
| B、CO(NH2)2 |
| C、KSCN |
| D、CHCl3 |
 用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( )
用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( ) X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:


