题目内容
16.如图为实验室制取少量乙酸乙酯的装置图,下列关于该实验的叙述中,不正确的是( )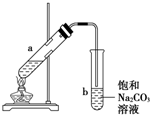
| A. | 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 | |
| B. | 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象 | |
| C. | 实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率 | |
| D. | 长玻璃导管只有导气的作用 |
分析 先加乙醇,后加浓硫酸,最后加冰醋酸,乙醇与乙酸发生酯化反应生成乙酸乙酯,为可逆反应,试管b中为饱和碳酸钠,可吸收乙醇、除去乙酸、降低乙酸乙酯的溶解度,导管在碳酸钠溶液的液面上,可防止倒吸,长导管可冷凝回流、导气,以此来解答.
解答 解:A.向a试管中先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸,试剂顺序不合理,故A错误;
B.因乙酸、乙醇均易溶于水,则试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象,故B正确;
C.反应为可逆反应,升高温度加快反应速率,则实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率,故C正确;
D.长玻璃导管起冷凝回流、导气作用,故D错误;
故选AD.
点评 本题考查有机物的制备实验,为高频考点,把握物质的性质、制备原理、实验装置及实验技能为解答的关键,侧重分析与实验能力的考查,注意长导管的作用,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
8.向X的溶液中,加入Y试剂,产生的沉淀示意图如图所示情形的是(注意线段的斜率)( )
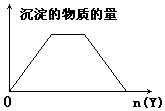

| A. | 向NaOH和Ca(OH)2的混合液中通入CO2 | |
| B. | 向HCl和AlCl3的混合液中滴加NaOH | |
| C. | 向NH4Cl和AlCl3的混合液中滴加NaOH | |
| D. | 向含NaOH的NaAlO2溶液中滴加盐酸 |
6.葡萄糖酸锌[(C6H11O6O)2Zn]是一种营养锌强化剂,对婴儿及青少年的智力和身体发育有重要作用.工业上通过如下两步制备:

(1)步骤一:充分反应后,过滤除去CaSO4沉淀.设计一个简单的实验,检验产物葡萄糖酸溶液中是否含有SO42-:取少量溶液于试管中,滴加BaCl2溶液,若产生白色沉淀,则说明含有SO42-.反之,说明不含SO42-
(2)步骤二:将葡萄糖酸溶液与ZnO混合,使其充分反应后,继续加入葡萄糖酸溶液至pH为5.8,其目的是抑制Zn2+的水解 ,下列物质可替代ZnO的是b(填字母).
a.NH3•H2O b.Zn(OH)2 c.NaOH d.ZnSO4
(3)将最后所得溶液浓缩至原来体积的$\frac{1}{3}$,加入适量无水乙醇,放置8h以上,经结晶、分离、干燥获得葡萄糖酸锌晶体.分离过程中加入无水乙醇的目的是降低葡萄糖酸锌的溶解度,有利于其结晶析出.
(4)下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
某研究性学习小组欲用粗制硫酸锌溶液(其中含有Fe2+、Cu2+等)制备出活性ZnO,然后再合成葡萄糖酸锌.实验室制备活性ZnO的步骤如下:
①取样,加入适量的KMnO4溶液,微热,调节溶液pH至3.2~5.2 (填写范围),除去溶液中Fe元素.
②加入过量的锌粉,过滤,向滤渣中加入适量稀硫酸,继续过滤,将两次滤液合并得较高纯度的硫酸锌溶液.
③将纯碱慢慢加入上述硫酸锌溶液中,得碱式碳酸锌[其化学式为Zn2(OH)2CO3],同时有无色气体产生.写出该反应的离子方程式:2CO32-+2Zn2++H2O=Zn2(OH)2CO3↓+CO2↑.
④过滤、洗涤,将沉淀灼烧得活性氧化锌.其中灼烧需要的主要仪器有:酒精灯、玻璃棒、三脚架、泥三角、坩埚、坩埚钳等.

(1)步骤一:充分反应后,过滤除去CaSO4沉淀.设计一个简单的实验,检验产物葡萄糖酸溶液中是否含有SO42-:取少量溶液于试管中,滴加BaCl2溶液,若产生白色沉淀,则说明含有SO42-.反之,说明不含SO42-
(2)步骤二:将葡萄糖酸溶液与ZnO混合,使其充分反应后,继续加入葡萄糖酸溶液至pH为5.8,其目的是抑制Zn2+的水解 ,下列物质可替代ZnO的是b(填字母).
a.NH3•H2O b.Zn(OH)2 c.NaOH d.ZnSO4
(3)将最后所得溶液浓缩至原来体积的$\frac{1}{3}$,加入适量无水乙醇,放置8h以上,经结晶、分离、干燥获得葡萄糖酸锌晶体.分离过程中加入无水乙醇的目的是降低葡萄糖酸锌的溶解度,有利于其结晶析出.
(4)下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 5.2 | 6.4 |
①取样,加入适量的KMnO4溶液,微热,调节溶液pH至3.2~5.2 (填写范围),除去溶液中Fe元素.
②加入过量的锌粉,过滤,向滤渣中加入适量稀硫酸,继续过滤,将两次滤液合并得较高纯度的硫酸锌溶液.
③将纯碱慢慢加入上述硫酸锌溶液中,得碱式碳酸锌[其化学式为Zn2(OH)2CO3],同时有无色气体产生.写出该反应的离子方程式:2CO32-+2Zn2++H2O=Zn2(OH)2CO3↓+CO2↑.
④过滤、洗涤,将沉淀灼烧得活性氧化锌.其中灼烧需要的主要仪器有:酒精灯、玻璃棒、三脚架、泥三角、坩埚、坩埚钳等.

 .
.
 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.