题目内容
下列溶液中各微粒的浓度关系正确的是( )
分析:A.从影响盐类水解的因素分析;
B.溶液呈碱性,应为c(OH-)>c(H+);
C.根据溶液的电荷守恒判断;
D.根据物料守恒判断.
B.溶液呈碱性,应为c(OH-)>c(H+);
C.根据溶液的电荷守恒判断;
D.根据物料守恒判断.
解答:解:A.物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液,c(NH4+):c[(NH4)2SO4]>c(NH4Cl),与NH4HSO4对比,NH4HSO4溶液中氢离子抑制铵根离子的水解,则c(NH4HSO4)>c(NH4Cl),则c(NH4+):c[(NH4)2SO4]>c(NH4HSO4)>c(NH4Cl),故A正确;
B.向NaCN溶液中加入适量HCN,得到的碱性混合溶液,应为c(OH-)>c(H+),故B错误;
C.酸式盐NaHA溶液中存在电荷守恒,应为c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),故C错误;
D.1.0mol?L-1 Na2CO3溶液中存在物料守恒:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D错误.
故选A.
B.向NaCN溶液中加入适量HCN,得到的碱性混合溶液,应为c(OH-)>c(H+),故B错误;
C.酸式盐NaHA溶液中存在电荷守恒,应为c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),故C错误;
D.1.0mol?L-1 Na2CO3溶液中存在物料守恒:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D错误.
故选A.
点评:本题考查离子浓度的大小比较,侧重于盐类水解和弱电解质的电离特点的考查,注意结合电荷守恒以及物料守恒解答该题,题目难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
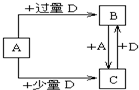 W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高.试回答下列各题:
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高.试回答下列各题: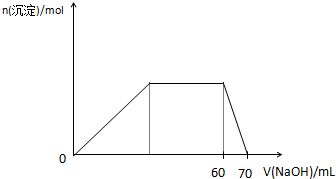 (2011?湖北模拟)X、Y、Z、M、N、K是由短周期元素构成的微粒,其中X、Y、Z是阳离子,M、N是中性分子,K是阴离子,它们具有下列结构特点和性质:
(2011?湖北模拟)X、Y、Z、M、N、K是由短周期元素构成的微粒,其中X、Y、Z是阳离子,M、N是中性分子,K是阴离子,它们具有下列结构特点和性质:

