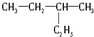
题目内容
醇X蒸气的密度是相同条件下H2密度的30.0倍,取1.20gX与过量的金属钠完全作用后生成224mL(标况)气体.取一定质量的X完全燃烧后,产生的气体依次通过浓硫酸和碱石灰,使两者的质量分别增加1.44g和2.64g.试求:
(1)通过计算确定X的分子式;
(2)写出X所有同分异构体的结构简式. .
(1)通过计算确定X的分子式;
(2)写出X所有同分异构体的结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)根据该醇与氢气的相对密度计算出其摩尔质量,再计算出1.20g醇的物质的量;根据二氧化碳、水的质量计算出物质的量,根据质量守恒计算出氧元素的质量、物质的量,最后计算出该醇的分子式;
(2)根据醇的物质的量、醇与钠反应生成氢气的物质的量确定含有羟基的数目,然后写出结构简式.
(2)根据醇的物质的量、醇与钠反应生成氢气的物质的量确定含有羟基的数目,然后写出结构简式.
解答:
解:(1)醇X蒸气的密度是相同条件下H2密度的30.0倍,则该醇的摩尔质量为:2g/mol×30.0=60g/mol,
1.20g该醇的物质的量为:n=
=0.02mol,
浓硫酸增重的为水的质量,1.44g水的物质的量为:n(H2O)=
=0.08mol,则n(H)=0.16mol,m(H)=1g/mol×0.16mol=0.16g,
碱金属增重的2.64g为二氧化碳的质量,则二氧化碳的物质的量为:n(CO2)=
=0.06mol,则n(C)=0.06mol,m(C)=12g/mol×0.06mol=0.72g,
1.2g醇中含有氧原子的质量为:m(O)=1.2g-0.16g-0.72g=0.32g,则n(O)=
=0.02mol,
该醇分子中含有C、H、O原子的数目分别为:
=3、
=8、
=1,
该醇的分子式为:C3H8O,
故答案为:C3H8O;
(2)分子式为C3H8O有机物的同分异构体有:2-丙醇:CH3CH(OH)CH3、1-丙醇:CH3CH2CH2OH和醚:CH3OCH2CH3,
故答案为:CH3CH(OH)CH3、CH3CH2CH2OH、CH3OCH2CH3.
1.20g该醇的物质的量为:n=
| 1.2g |
| 60g/mol |
浓硫酸增重的为水的质量,1.44g水的物质的量为:n(H2O)=
| 1.44g |
| 18g/mol |
碱金属增重的2.64g为二氧化碳的质量,则二氧化碳的物质的量为:n(CO2)=
| 2.64g |
| 44g/mol |
1.2g醇中含有氧原子的质量为:m(O)=1.2g-0.16g-0.72g=0.32g,则n(O)=
| 0.32g |
| 16g/mol |
该醇分子中含有C、H、O原子的数目分别为:
| 0.06mol |
| 0.02mol |
| 0.16mol |
| 0.02mol |
| 0.02mol |
| 0.02mol |
该醇的分子式为:C3H8O,
故答案为:C3H8O;
(2)分子式为C3H8O有机物的同分异构体有:2-丙醇:CH3CH(OH)CH3、1-丙醇:CH3CH2CH2OH和醚:CH3OCH2CH3,
故答案为:CH3CH(OH)CH3、CH3CH2CH2OH、CH3OCH2CH3.
点评:本题考查了有机物分子式、结构简式的确定,题目难度中等,注意掌握有机物分子式、结构简式的计算方法,明确质量守恒定律在确定有机物分子式中的应用方法.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列说法不正确的是( )
| A、Fe2O3俗称铁红,常用作红色油漆和涂料 |
| B、Na2SiO3俗称水玻璃,是制备硅胶和木材防火剂的原料 |
| C、CH3COOH俗称醋酸,是食醋的主要成分 |
| D、SiC俗称金刚砂,可用作砂纸、砂轮的磨料 |
 的分子式是
的分子式是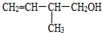 .该有机物中所含官能团的名称是
.该有机物中所含官能团的名称是

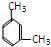 和
和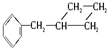
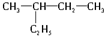 和
和 
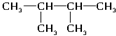 和
和