题目内容
运用元素周期律分析下面的推断,其中错误的是( )
A.铍(Be)是一种轻金属,其氧化物对应的水化物可能具有两性
B.砹是一种有色固体,HAt很不稳定,AgAt是有色难溶于水且感光性很强的固体
C.第三周期元素的离子半径从左到右依次减小
D.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体
C
【解析】
试题分析:铍和铝都是位于金属元素和非金属元素交界线附近的元素,既有一定的金属性,又有一定的非金属性,它们的氧化物和氧化物对应的水化物都具有两性,A正确;根据卤素的相关知识可推知砹是一种有色固体(F2→I2颜色加深),HAt很不稳定(HF→HI稳定性减弱),AgAt是有色难溶于水且感光性很强的固体(由氯化银、溴化银、碘化银类比推知),B正确;同一周期元素的原子形成离子时,阳离子电子层少于阴离子,半径小,C错误;由硫酸钡是难溶于水和盐酸的白色固体类比推出硫酸锶(SrSO4)也是难溶于水和盐酸的白色固体,D正确。
考点:元素周期表、元素周期率。

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、烃分子中的碳原子与其他原子的结合方式一定是通过非极性键 | B、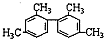 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | C、聚乙烯能使溴水褪色 | D、软脂酸和油酸互为同系物 |
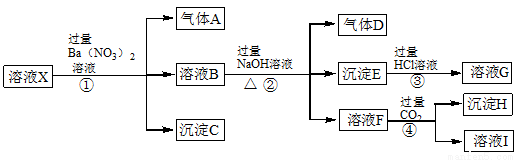


 ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )
