题目内容
| |||||||||||||||||||
答案:
解析:
解析:
(1) |
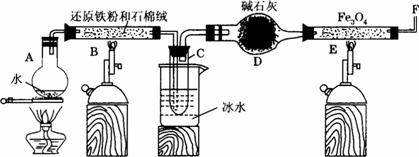
防止液体暴沸(2分),冷凝水蒸气(2分) |
(2) |
检验氢气的纯度(2分),点燃氢气(2分) |
(3) |
实验中不断通入水蒸气增大反应物浓度,并移走氢气减小生成物浓度,从而使反应正向进行(2分) |
(4) |
取滤液少量,向其中滴加KSCN溶液,溶液变为血红色,即证明含有Fe3+(2分) |

练习册系列答案
相关题目

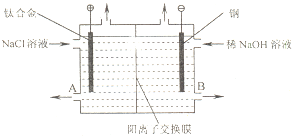 电解食盐水使用的离子交换膜电解槽装置如图所示.经过净化精制的饱和食盐水不断送入阳极室,向阴极室不断加入稀NaOH溶液.阳离子交换膜具有很好的选择性,它只允许阳离子通过.
电解食盐水使用的离子交换膜电解槽装置如图所示.经过净化精制的饱和食盐水不断送入阳极室,向阴极室不断加入稀NaOH溶液.阳离子交换膜具有很好的选择性,它只允许阳离子通过.