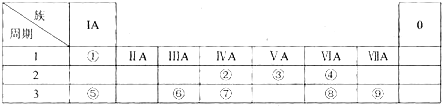
题目内容
(1)下列实验操作中错误的是
A.做焰色反应的铂丝,用硫酸洗涤后,再在酒精灯火焰上灼烧至无色,才可使用
B.向溶液中加盐酸酸化的BaCl2,如果产生白色沉淀,则一定有SO42-
C.可用稀盐酸一次区别开Na2SO4、AgNO3 和Na2CO3三种溶液
D.除去硝酸钾固体中混有的少量氯化钾,所进行的实验步骤依次是:配成较高温度下的浓溶液、蒸发结晶、过滤
E.用灼烧法鉴别棉织品和毛织品,有焦臭味的是毛织品
F.从含碘单质的有机溶液中提取碘单质和回收有机溶液,还需要经过蒸馏
(2)有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验.①将该粉末溶于水得无色溶液和白色沉淀;②在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;③取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰.
由上述现象可推断:一定有 ,可能有 .
A.做焰色反应的铂丝,用硫酸洗涤后,再在酒精灯火焰上灼烧至无色,才可使用
B.向溶液中加盐酸酸化的BaCl2,如果产生白色沉淀,则一定有SO42-
C.可用稀盐酸一次区别开Na2SO4、AgNO3 和Na2CO3三种溶液
D.除去硝酸钾固体中混有的少量氯化钾,所进行的实验步骤依次是:配成较高温度下的浓溶液、蒸发结晶、过滤
E.用灼烧法鉴别棉织品和毛织品,有焦臭味的是毛织品
F.从含碘单质的有机溶液中提取碘单质和回收有机溶液,还需要经过蒸馏
(2)有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验.①将该粉末溶于水得无色溶液和白色沉淀;②在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;③取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰.
由上述现象可推断:一定有
考点:化学实验方案的评价,物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:(1)A.硫酸不挥发,干扰离子检验;
B.应先加盐酸,排除其他离子的干扰;
C.Na2SO4、AgNO3 和Na2CO3三种溶液分别与盐酸混合的现象为:无现象、白色沉淀、气体生成;
D.蒸发结晶,硝酸钾、氯化钾均析出;
E.毛织品的成分为蛋白质,灼烧有烧焦羽毛的气味;
F.碘与有机溶剂的沸点不同;
(2)由①将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由②在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
综上所述:原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2;一定不含有CuCl2、K2CO3、K2SO4;可能含有NaCl,以此来解答.
B.应先加盐酸,排除其他离子的干扰;
C.Na2SO4、AgNO3 和Na2CO3三种溶液分别与盐酸混合的现象为:无现象、白色沉淀、气体生成;
D.蒸发结晶,硝酸钾、氯化钾均析出;
E.毛织品的成分为蛋白质,灼烧有烧焦羽毛的气味;
F.碘与有机溶剂的沸点不同;
(2)由①将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由②在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
综上所述:原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2;一定不含有CuCl2、K2CO3、K2SO4;可能含有NaCl,以此来解答.
解答:
解:(1)A.硫酸不挥发,干扰离子检验,应利用稀盐酸洗涤,故A错误;
B.应先加盐酸,排除其他离子的干扰,再加氯化钡检验硫酸根离子,故B错误;
C.Na2SO4、AgNO3 和Na2CO3三种溶液分别与盐酸混合的现象为:无现象、白色沉淀、气体生成,现象不同,可一次性鉴别,故C正确;
D.蒸发结晶,硝酸钾、氯化钾均析出,应利用结晶法除杂,故D错误;
E.毛织品的成分为蛋白质,灼烧有烧焦羽毛的气味,则用灼烧法可鉴别,故E正确;
F.碘与有机溶剂的沸点不同,则提取碘单质和回收有机溶液,还需要经过蒸馏,故F正确;
故答案为:ABD;
(2)由①将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由②在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
由上述分析可知,原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2,一定不含有CuCl2、K2CO3、K2SO4,可能含有NaCl,
故答案为:Na2CO3、Na2SO4、Ba(NO3)2;NaCl.
B.应先加盐酸,排除其他离子的干扰,再加氯化钡检验硫酸根离子,故B错误;
C.Na2SO4、AgNO3 和Na2CO3三种溶液分别与盐酸混合的现象为:无现象、白色沉淀、气体生成,现象不同,可一次性鉴别,故C正确;
D.蒸发结晶,硝酸钾、氯化钾均析出,应利用结晶法除杂,故D错误;
E.毛织品的成分为蛋白质,灼烧有烧焦羽毛的气味,则用灼烧法可鉴别,故E正确;
F.碘与有机溶剂的沸点不同,则提取碘单质和回收有机溶液,还需要经过蒸馏,故F正确;
故答案为:ABD;
(2)由①将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由②在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
由上述分析可知,原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2,一定不含有CuCl2、K2CO3、K2SO4,可能含有NaCl,
故答案为:Na2CO3、Na2SO4、Ba(NO3)2;NaCl.
点评:本题考查化学实验方案的评价及物质检验和鉴别,为高频考点,把握物质的性质及实验现象为解答的关键,侧重分析推断能力及知识综合应用能力的考查,注意常见离子的检验方法,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
同位素Si中发现新的物理学“幻数”,下列有关
Si的说法不正确的是( )
42 14 |
A、
| ||
B、
| ||
C、
| ||
D、
|
25℃时,将两个铂电极插入一定量的Na2SO4饱和溶液中进行电解.通电一段时间后,在阴极逸出a mol气体,同时有W g Na2SO4?10H2O晶体析出.若温度保持不变,剩余溶液中溶质的质量分数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在101kPa和298K时,有关反应的热化学方程式有:下列说法错误的是( )
H2(g)+
O2(g)═H2O(g)△H1=-241.8kJ?mol-1
H2(g)+
O2(g)═H2O(l)△H2=-285.8kJ?mol-1.
H2(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
| A、H2燃烧生成1mol H2O(g)时,放出241.8kJ的热量 | ||
B、O2前面的
| ||
| C、燃烧热是以在101kPa时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8kJ?mol-1 | ||
| D、1mol液态水变成水蒸气时吸收44kJ的热量 |
下列各溶液中,各离子可能大量共存的有( )
| A、含有大量Ba2+的溶液中:HCO3-、Fe3+、Ag+、SO42-、SCN- |
| B、滴加无色酚酞试液后为红色的溶液中:Na+、CO32-、K+、ClO-、AlO2- |
| C、由水电离的c(OH-)=10-14mol?L-1 的溶液中:CH3COO-、C6H5O-、Na+、K+ |
| D、加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl-、HS- |