题目内容
16.有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是( )| A. | 物质的量之比为1:1 | B. | 物质的量之比为1:2 | ||
| C. | 质量之比为4:1 | D. | 质量之比为2:1 |
分析 只有硅和NaOH溶液反应生成氢气,铁与HCl反应生成氢气,根据生成氢气的量计算粗硅中铁和硅的物质的量之比.
解答 解:根据电子得失:可知铁与盐酸反应:Fe~~H2,而硅与氢氧化钠反应:Si~~2H2,放出等量的H2,设生成氢的量为2mol,所以粗硅中铁和硅的物质的是之比为:2:1,质量之比为:2×56:1×28=4:1,故选:C.
点评 本题考查混合物反应的计算,侧重考查学生分析、计算能力,明确只有Si和NaOH溶液反应是解本题关键,利用关系式解答即可,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
6.离子方程式2Ca2++3HCO3-+3OH-═2CaCO3↓+CO32-+3H2O可以表示( )
①Ca(HCO3)2与NaOH溶液反应
②NaHCO3与澄清石灰水反应
③Ca(HCO3)2与澄清石灰水反应
④NH4HCO3与澄清石灰水反应.
①Ca(HCO3)2与NaOH溶液反应
②NaHCO3与澄清石灰水反应
③Ca(HCO3)2与澄清石灰水反应
④NH4HCO3与澄清石灰水反应.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①② |
7.下列现象与胶体无关的是( )
| A. | 豆浆中加入石膏制豆腐 | |
| B. | 晚上,打开手电筒看到一条明亮的光路 | |
| C. | 用“血透”法治疗肾病患者 | |
| D. | 二氧化碳使澄清石灰水变浑浊 |
1.下列离子方程式正确的是( )
| A. | 苏打溶液与稀盐酸反应的离子反应方程式:HCO3-+H+═CO2↑+H2O | |
| B. | Fe2O3与HI:Fe2O3+6H+═2Fe3++3H2O | |
| C. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 浓烧碱溶液中加入铝片:Al+OH-+H2O═AlO2-+H2↑ |
8.实验室有一瓶久置的白色K2SO3粉末,为确定其是否被氧化及其成分,下列结论错误的是( )
| A. | 将粉末溶于水,加入Ba(NO3)2,再加过量盐酸,有白色沉淀生成不能证明原粉末被氧化 | |
| B. | 粉末在空气中变质被氧化的方程式:2K2SO3+O2═2K2SO4 | |
| C. | 将粉末溶于水,加入氯化钡和过量的盐酸,有白色沉淀和气泡生成,证明原粉末是K2SO4和K2SO3的混合物 | |
| D. | 元素分析表明粉末中K和S元素的质量比为39:16,推测该粉末为纯净物 |
5.下列变化或过程中发生化学变化的是( )
| A. | 氮的固定 | |
| B. | 实验室中制取蒸馏水 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集 | |
| D. | 用铂丝蘸取NaCl溶液进行焰色反应 |
19.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | 向次氯酸钙溶液通入足量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |

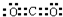 ;写出X、Y之间反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2;
;写出X、Y之间反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2;