题目内容
下列电离方程式书写正确的是( )
分析:用化学式和离子符号表示电离过程的式子,称为电离方程式,电离方程式中,弱电解质的电离用“?”,强电解质的电离用“=”,注意弱酸的酸根离子不能拆分,并遵循电荷守恒、质量守恒定律,以此来解答.
解答:解:A、碳酸氢钠为强电解质,溶液中电离出碳酸氢根离子和钠离子,其电离方程式为:NaHCO3═Na++HCO3-,故A错误;
B、硫化氢是二元弱酸,电离分步进行,主要以第一步电离为主,正确电离方程式为:H2S?H++HS-,故B错误;
C、硫酸氢钠为强电解质,溶液中完全电离,应该用“=”,不写磷酸氢根离子的电离,正确的电离方程式为:Na2HPO4═2Na++HPO42-,故C错误;
D、水是弱电解质,存在电离平衡,用“?”,水的电离方程式为:2H2O?H3O++OH?,故D正确;
故选D.
B、硫化氢是二元弱酸,电离分步进行,主要以第一步电离为主,正确电离方程式为:H2S?H++HS-,故B错误;
C、硫酸氢钠为强电解质,溶液中完全电离,应该用“=”,不写磷酸氢根离子的电离,正确的电离方程式为:Na2HPO4═2Na++HPO42-,故C错误;
D、水是弱电解质,存在电离平衡,用“?”,水的电离方程式为:2H2O?H3O++OH?,故D正确;
故选D.
点评:本题考查电离方程式的书写判断,题目难度不大,明确书写方法及弱酸根离子的书写是解答的关键,注意B项为解答的易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
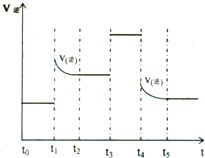 (2009?安徽模拟)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题:
(2009?安徽模拟)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题: